《中考化学热点专题精讲与突破:7大科技前沿真题演练》
(文末附下载及答案)
1.化学真题精讲 | 氢能:中考“能源”专题核心突破
【原题材料】
加快能源转型升级,发展新质生产力。氢气是最理想的清洁能源,依据不同制取方式,可分为“绿氢”“灰氢”“蓝氢”“紫氢”和“金氢”等。题图带你认识“多彩”的氢。
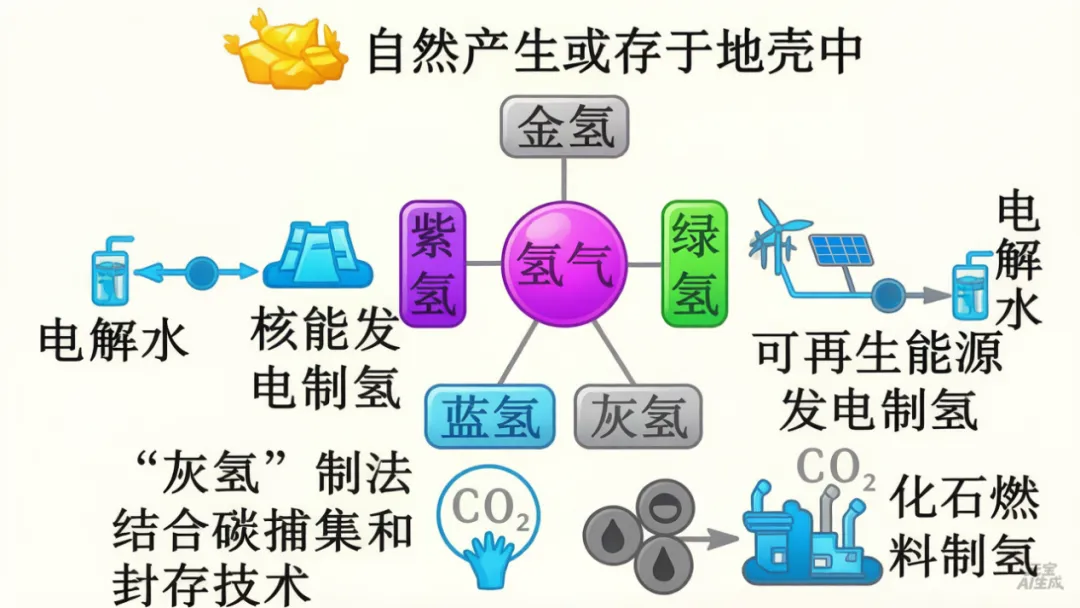
储氢是实现氢能广泛应用的重要环节,分为物理储氢和化学储氢,前者包括高压气态、低温液态、吸附等储存方式,后者将氢气转化为其他化合物进行储存。“液氨储氢”的原理是氢气与氮气在一定条件下生成液氨,进行储存。
【考点闯关】
依据上文,回答问题:
1.电解水制氢的化学方程式为_____________。
2.属于“绿氢”和“紫氢”的分别是______和______(填字母)。
a.风能发电制氢 b. 煤燃烧发电制氢 c. 核能发电制氢
3.从微观角度解释,氢气能被压缩储存的原因是______________。
4.将氢气降温液化进行储存,属于物理储氢中的__________储存方式。
5.“液氨储氢”属于________(填“物理”或“化学”)储氢。
6.写出氢能的一种应用:__________________。

2.揭秘“非核氢弹”——化学能驱动的高能材料
[原题材料]
2025年,我国科研机构成功试爆了一款新型高能装置,被外媒称为“非核氢弹”。该装置仅重2公斤,其核心装药是固态储氢材料——氢化镁(MgH2)。
其工作原理是:通过常规炸药提供初始热量,引发氢化镁的剧烈热分解反应,生成金属镁和氢气;随后氢气迅速与氧气燃烧。这种“分解-燃烧”的链式反应,能在瞬间产生超过1000℃的高温火球,威力可达同质量TNT炸药的15倍,且爆炸后完全不产生放射性污染。
在设想应用中,其高温热流可用于熔毁特定目标,实现高效毁伤。
【考点闯关】
依据上文,回答问题:
1.该装置能量的最终来源是______(填“化学能”或“核能”)。
2.氢化镁(MgH2)受热分解的化学方程式为______。
3.下列有关该装置的描述,正确的一项是()。
A. 其爆炸过程涉及原子核的变化
B. 其能量释放属于物理变化
C. 氢气燃烧是其释放热量的主要反应之一
D. 其所有产物均具有放射性
4.该装置爆炸后,其产物中可能含有______(写一种即可),但绝不会含有放射性物质。
5.与核武器相比,该技术被称为“非核”的最主要依据是______。

3.中考热点聚焦:动力电池的未来——固态电池技术
[原题材料]
随着新能源汽车的快速发展,提升动力电池的能量密度与安全性成为行业核心课题。固态电池,作为下一代电池技术,正从实验室走向产业化。
传统锂电池内部填充有易燃的液态有机电解液,是热失控起火的主要诱因。固态电池的革命性在于,用不可燃的固态电解质(如硫化物固态电解质Li₃PS₄)完全取代了液态电解液,从根本上杜绝了电池因内部短路而起火爆炸的可能,实现了本质安全。
固态电池在生产与回收过程中,涉及含锂化合物的转化。例如,其关键材料之一的氢氧化锂(LiOH)是一种碱,能与空气中或系统内的二氧化碳反应,生成碳酸锂(Li₂CO₃)和水。这一性质也被考虑用于电池系统的安全防护设计。
此外,固态电解质具有极高的机械强度,能有效抑制充放电过程中锂枝晶的生长。这使得直接使用超高容量的金属锂(Li)作为负极成为可能,能量密度有望达到现有液态电池的2倍以上。近期,我国科研团队在固-固界面离子传输等关键技术上取得了突破。
【考点闯关】
依据上文,回答问题:
1.固态电池实现“本质安全”的核心是使用______取代了传统锂电池中易燃的液态电解液。
2.固态电池能使用金属锂作负极,主要得益于固态电解质能有效()。
A. 降低电池成本B. 抑制锂枝晶生长
C. 拓宽工作温度D. 提高充电速度
3.文中提到,氢氧化锂(LiOH)可用于吸收二氧化碳,反应生成碳酸锂(Li₂CO₃)和水。请写出该反应的化学方程式:______。
4.根据文中信息,下列关于固态电池的描述,不正确的是( )。
A. 其能量密度远高于传统液态电池
B. 其技术难点之一是固-固界面离子传输
C. 我国科研已通过“钠离子”掺杂解决了界面问题
D. 其固态电解质不可燃,安全性高
5.固态电池有望使用的一种高容量负极材料是______。

4.中考热点聚焦:从玉米到环保塑料
[原题材料]
塑料制品在带来便利的同时,也因其难以降解引发了严重的“白色污染”问题。科学家们从大自然中寻找灵感,将目光投向了可再生资源——玉米。玉米粒中富含淀粉,这是一种糖类物质。通过生物发酵等工艺,可从玉米淀粉中制取乳酸,再将乳酸聚合,便可制成一种新型生物可降解材料——聚乳酸,俗称“玉米塑料”。
“玉米塑料”最大的优势在于其出色的可降解性。废弃后,在特定条件下可被自然界中的微生物完全分解,最终产物是二氧化碳和水,从而重新进入自然界的碳循环,不会像传统塑料那样在环境中长期存留。在制备“玉米塑料”的过程中,提取玉米淀粉是关键步骤,常采用湿法提取工艺。研究人员在特定温度(如50℃)和特定成分的浸泡液中,研究了浸泡时间对玉米淀粉提取率的影响,其变化趋势如题图所示。
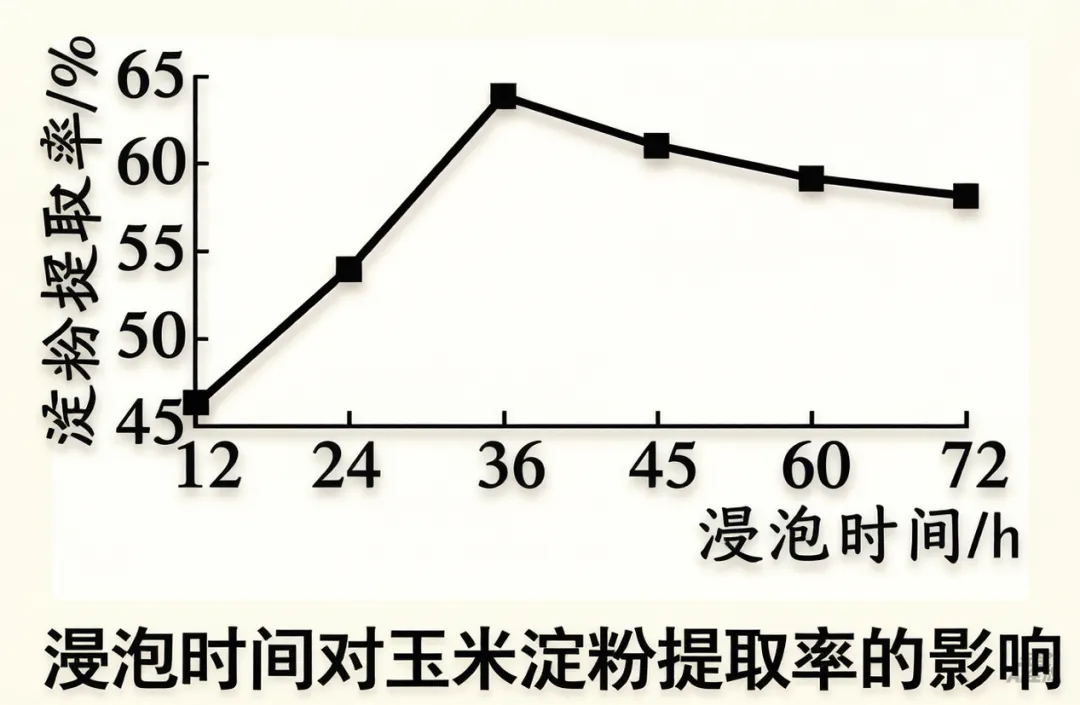
除了制造环保塑料,玉米的另一大用途是酿酒。玉米中的淀粉经过发酵可以转化为酒精。酒精不仅在工业和生活中有广泛应用,其完全燃烧的产物也是二氧化碳和水,是一种清洁的燃料。
【考点闯关】
依据上文,回答问题:
1.玉米中富含的主要营养物质淀粉属于六大营养素中的 ______(填“糖类”或“蛋白质”)。
2.与传统石油基塑料相比,玉米塑料的环保优势在于,其废弃后可被微生物最终分解为 ______和 ______,从而参与自然界碳循环。
3.从玉米淀粉到聚乳酸,发生了 ______(填“物理”或“化学”)变化,理由是 ______。
4.酒精(化学式为C2H5OH)在空气中完全燃烧的化学方程式为 ______。
5.在玉米淀粉的湿法提取实验中,若其他条件不变,仅延长浸泡时间,淀粉提取率的变化趋势最可能是 ______(填字母)。
a. 持续快速升高b. 先升高后趋于稳定
c. 始终保持不变d. 持续降低

5.中考热点聚焦:茶叶中的“健康卫士”——茶多酚
[原题材料]
中华“茶文化”源远流长。茶叶中含有大量茶多酚。茶多酚是茶叶中多酚类物质的总称,为白色粉末,具有吸水性,易溶于温水、乙醇,味苦涩,在碱性环境中不稳定。研究表明,茶多酚具有抗氧化、延缓衰老、降血脂和降血糖等健康功能。
不同种类茶叶的茶多酚含量因其发酵程度不同而有显著差异。具体测定结果如下表所示:
样品名称 | 绿茶 | 白茶 | 黄茶 | 青茶 | 红茶 | 黑茶 |
发酵程度 | 未发酵 | 微发酵 | 轻发酵 | 半发酵 | 全发酵 | 后发酵 |
茶多酚含量 | 54.79% | 32.53% | 32.33% | 20.04% | 17.36% | 17.08% |
研究人员进一步选用绿茶与白茶,提取不同浓度的茶多酚提取液,进行总抗氧化能力(FRAP)实验,并与高效抗氧化剂Vc进行对比,结果如图所示。
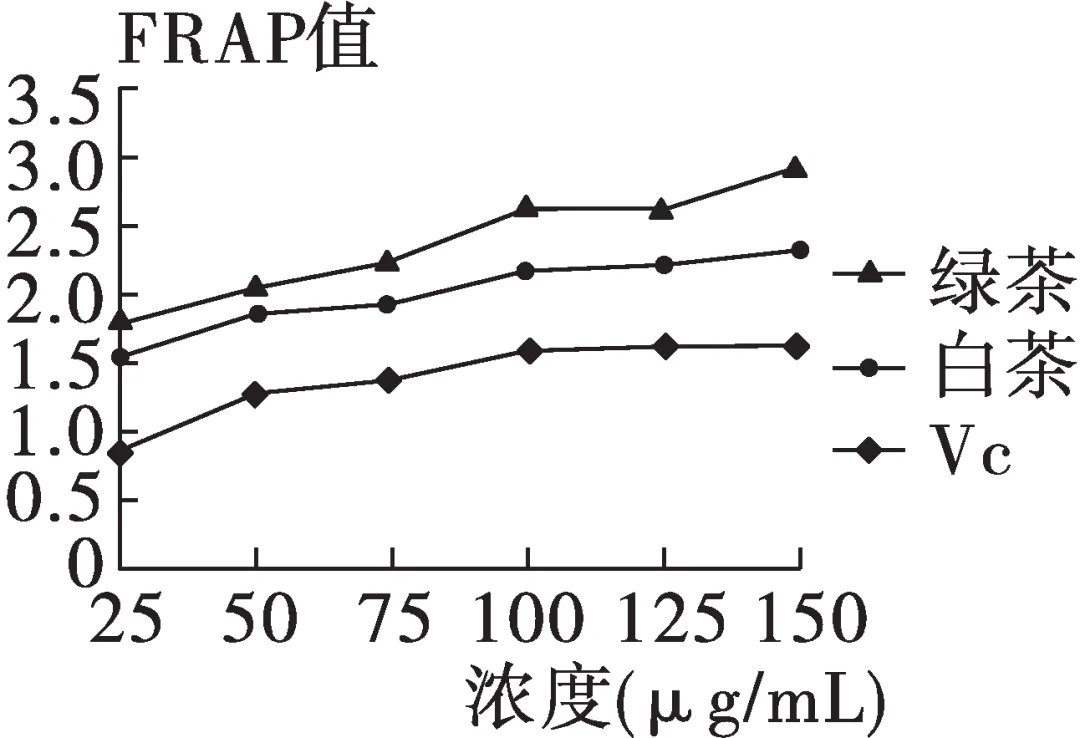
实验表明,茶多酚具有较好的抗氧化活性,是人体自由基的清除剂,有助于延缓衰老。日常生活中,茶汤越浓、越苦涩、回甘越好,通常意味着茶多酚浓度越高。
【考点闯关】
依据上文,回答问题:
1.茶多酚的物理性质包括:白色粉末、有吸水性、易溶于温水和乙醇、味 ______。
2.为促进茶叶生长,可施用硫酸钾(K2SO4),它属于 ______(填“氮”“磷”或“钾”)肥。
3.根据表格数据分析,绿茶中茶多酚含量远高于其他茶类,其主要原因是绿茶的 ______程度最低。
4.对比绿茶、白茶提取液与Vc的FRAP实验曲线(图略),可以得出的结论是:在茶多酚提取液浓度相同时,______的总抗氧化能力最强。
5.某种茶多酚(化学式为C6H6O2)在一定条件下被氧化,生成两种常见的无毒无害氧化物(二氧化碳和水),该反应的化学方程式为 ______。

6.中考热点聚焦:捕捉“温室元凶”——碳捕集与利用技术
[原题材料]
为实现“碳中和”目标,人类不仅需要减少二氧化碳(CO₂)排放,还需主动从大气或工业尾气中捕获并利用它,这项技术被称为“碳捕集、利用与封存”(CCUS)。
捕集是第一步。常用方法是利用碱性溶液(如氢氧化钠溶液)吸收CO₂。这是因为CO₂是一种酸性氧化物,能与碱反应生成盐和水。例如,用澄清石灰水[Ca(OH)₂溶液]检验CO₂,就是此原理的简单应用,反应会生成白色的碳酸钙(CaCO₃)沉淀。
利用是关键。捕获的CO₂并非“废物”,可转化为资源。在催化剂作用下,CO₂能与氢气反应,生成甲醇(CH₃OH)和水,其反应的微观示意图如下图所示。此外,CO₂还可注入温室促进植物光合作用,或用于生产碳酸饮料。
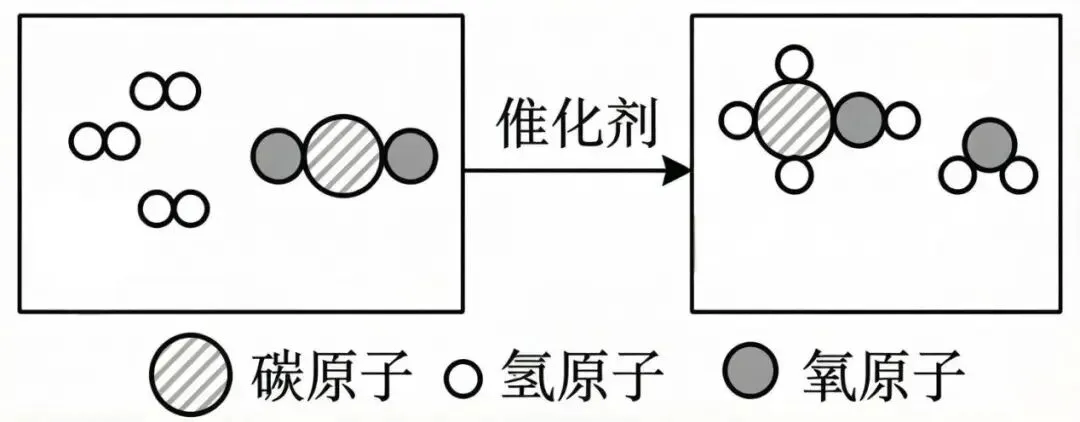
封存是最后手段,将超临界CO₂注入深层地质构造中永久储存。我国在燃煤电厂、水泥厂等排放源附近已开展多项CCUS示范项目。
【考点闯关】
依据上文,回答问题:
1.大气中CO₂含量过高,会导致______效应增强,加剧全球气候变化。
2.实现“碳中和”目标中的“碳”,主要是指( )。
A. 碳元素B. 二氧化碳
C. 碳单质D. 所有含碳物质
3.文中提及,可用氢氧化钠(NaOH)溶液吸收CO₂,其反应原理与CO₂的检验一样,请写出该反应的化学方程式:______。
4.请写出微观示意图中,二氧化碳与氢气在催化剂作用下反应生成甲醇(CH₃OH)的化学方程式:______。
5.“碳封存”可以减少二氧化碳排放,“碳封存”可将CO₂压缩至地下,转化为液态CO₂储存,其原因是:______(从微观角度解释)。

7.中考热点聚焦:生活中的化学——荧光棒的奥秘
[原题材料]
荧光棒,外形多为条状,外层以聚乙烯(PE)包装,内置一玻璃管夹层。其中的化学物质主要有三种:过氧化物、酯类化合物和荧光染料。
简单来说,其发光原理是:玻璃管夹层内外的过氧化物和酯类化合物发生化学反应,将反应后释放的能量传递给荧光染料,再由染料发出荧光。由于发光的同时几乎不产生热量,属于“冷光源”,因此发光的效率很高。
荧光棒的发光时间受温度和刚折时的亮度影响:环境温度越高,发光时间越短;刚折时的亮度越高,发光时间也越短。
荧光棒所发出的光是靠化学反应激发染料发出的非放射性光,不会伤害人体。但荧光棒中的化学成分如苯二甲酸二甲酯和苯二甲酸二丁酯,具有低毒性,如果误吸或触碰,可能造成恶心、头晕等现象。因此,正确的使用和保存方法非常重要。
【考点闯关】
依据上文,回答问题:
1.从材料分类看,荧光棒外层包装使用的聚乙烯(PE)属于 ______(填“天然材料”或“合成材料”)。
2.荧光棒发光时,其能量转化形式主要是将 ______能转化为光能。
3.下列关于荧光棒中成分苯二甲酸二甲酯(C₁₀H₁₀O₄)的说法,正确的是( )。
A. 它由碳、氢、氧三种原子构成
B. 其中碳元素和氢元素的质量比为1:1
C. 它是一种无机化合物
D. 一个C₁₀H₁₀O₄分子中共有24个原子
4.结合文中信息,下列有关荧光棒使用和保存的建议,不合理的是( )。
A. 为了延长发光时间,可在使用前将其冷藏
B. 发光过程中感觉微热是正常的,说明能量转化效率高
C. 应避免儿童拆解或啃咬,防止误食有毒物质
D. 废弃的荧光棒应作为有害垃圾处理,不应随意丢弃
5.夏天户外音乐会使用的荧光棒往往比冬天室内使用的发光时间短。请结合文中知识,解释这一现象:______。

【资料下载链接】(下载打印练习)







