




























制作过程中为了保证效率,经常用把前面已经做好的文字或动画效果进行复制粘贴,可能有部分内容没及时修改到位,若发现问题,欢迎指正,谢谢!


以下教学设计内容为利用AI根据课件生成
(一)情境导入:浣纱寻踪,初识古法制涤(5分钟)
1.视频激趣:播放古人浣纱的视频,展示现代人对古人洗衣“清水捶打”的刻版印象,提出问题:“事实上古人早已发明了专属的‘洗衣液’,能让衣服洗得更干净,这神秘的‘洗衣液’究竟是什么?”
2.史料佐证:展示《礼记·内则篇》中关于草木灰洗衣的记载,引出本节课的核心线索——洗涤剂的演进(草木灰→古法肥皂→爆炸盐)。
3.过渡引题:“从古代的草木灰到现代的爆炸盐,洗涤剂的配方在变,但背后的化学原理始终围绕酸碱盐的知识。今天我们就走进《浣纱中的化学》,沿着洗涤剂的演进之路,展开酸碱盐的大单元复习,解锁浣纱中的化学智慧!”
4.明确目标:板书课题《浣纱中的化学——基于洗涤剂演进的酸碱盐大单元复习》,呈现本节课的核心脉络:碱起—脂解—氧绽。
(二)模块一:碱起——草木灰,浣纱之初的化学智慧(10分钟)
过渡语:“草木灰是古人最易得的洗涤剂,沾有鞋油的抹布用草木灰浸出液能轻松洗净,这背后的化学奥秘是什么?草木灰浸出液为何能去污?让我们从实验开始探究!”
1.实验探究1:检验草木灰的洗涤效果与酸碱性
○分组实验:将沾有鞋油的抹布分别用清水、草木灰浸出液清洗,观察现象;用pH试纸、紫色石蕊试液检验草木灰浸出液的酸碱性。
○实验现象:清水洗抹布效果差,草木灰浸出液能洗净鞋油;pH试纸显蓝色(pH>7),石蕊试液变蓝。
○得出结论:草木灰浸出液呈碱性,碱性物质能去除油污,这是草木灰去污的核心原理。
2.实验探究2:设计实验证明草木灰中CO32−的存在
○提出问题:教材指出草木灰的主要成分是碳酸钾,如何用化学方法证明CO32−的存在?
○实验原理:CO32−与稀盐酸反应生成CO2,CO2能使澄清石灰水变浑浊。
○分组实验:向装有草木灰的饮料瓶中加入稀盐酸,旋紧瓶塞,将产生的气体通入盛有澄清石灰水的井穴板中。
○实验现象:加入稀盐酸后产生大量气泡,澄清石灰水变浑浊。
○得出结论:草木灰中含有CO32−,证明主要成分为碳酸钾(K2CO3)。
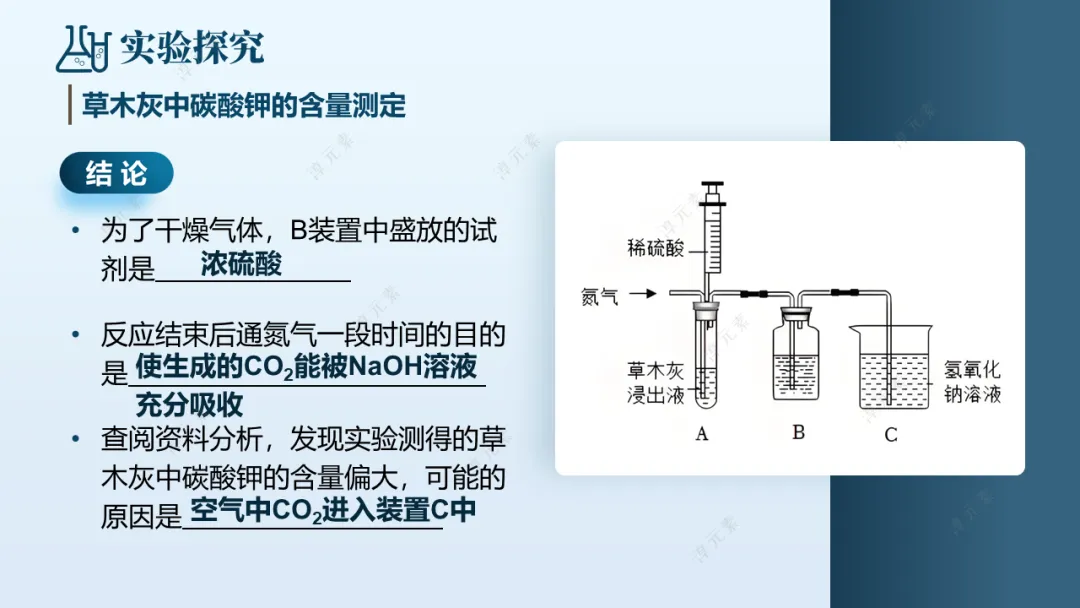
3.实验分析:草木灰中碳酸钾的含量测定与误差分析
○展示实验装置:草木灰浸出液与稀硫酸反应→装置B(干燥剂)→装置C(氢氧化钠溶液吸收CO2),反应后通氮气。
○问题串设计:
① 装置B中盛放的试剂是什么?(浓硫酸,作用是干燥CO2,防止水蒸气干扰)
② 反应结束后通氮气的目的是什么?(使生成的CO2全部被装置C的NaOH溶液吸收,减小实验误差)
③ 实验测得碳酸钾含量偏大,可能的原因是什么?(空气中的CO2进入装置C,被NaOH溶液吸收,导致测得的CO2质量偏大)
○归纳总结:碳酸盐含量测定的关键是准确收集并检验生成的CO2,排除外界因素的干扰。
(三)模块二:脂解——古法肥皂,浣纱之智的化学进阶(12分钟)
过渡语:“草木灰的去污能力有限,且仅能去除简单油污,古人在草木灰的基础上创新,结合贝壳灰制出了碱液,进而熬制出古法肥皂,这一过程藏着哪些酸碱盐的系列反应?肥皂为何能去除油脂,又为何遇硬水会失效?”
1.视频分析:古法制皂的工艺流程
○播放古法制皂视频,梳理核心步骤:制备碱液(草木灰水+贝壳灰)→炼油入碱(猪油+碱液加热搅拌)→成型晾干。
○提出问题:贝壳灰的主要成分是CaO,制备碱液的过程发生了哪些化学反应?
2.核心反应书写:碱液的制备
○学生自主书写,教师板书纠正:
① CaO+H2O=CaOH2(碱性氧化物与水反应生成碱)
② CaOH2+K2CO3=CaCO3↓+2KOH(碱与盐发生复分解反应生成新碱和新盐)
○强调:该反应是复分解反应,满足“生成沉淀”的条件,CaCO3沉淀的生成使反应能持续进行。
3.实验探究3:油脂的碱性水解与反应完全判断
○问题串设计:
① “炼油入碱”时不断搅拌的目的是什么?(使液态猪油与碱液充分接触,加快反应速率,使反应更充分)
② 如何判断油脂已完全反应?(油脂难溶于水且密度比水小,反应完全后上层无油状物质)
○原理讲解:油脂在碱性、加热条件下发生水解反应,生成可溶于水的物质,因此能去除油污,该反应也被称为“皂化反应”。
4.实验探究4:肥皂与硬水的反应,深挖复分解反应本质
○分组实验:将肥皂水分别加入氯化钙溶液、氯化镁溶液中,观察现象。
○实验现象:两种溶液中均产生白色沉淀,肥皂水失去去污能力。
○书写反应:结合硬脂酸钠(肥皂主要成分)的化学式,书写复分解反应方程式:
① 2C17H35COONa+CaCl2=C17H35COO2Ca↓+2NaCl
② 2C17H35COONa+MgCl2=C17H35COO2Mg↓+2NaCl
○微观分析:从离子角度看,硬脂酸根离子与Ca2+、Mg2+相互消耗生成沉淀,这是复分解反应的微观本质。
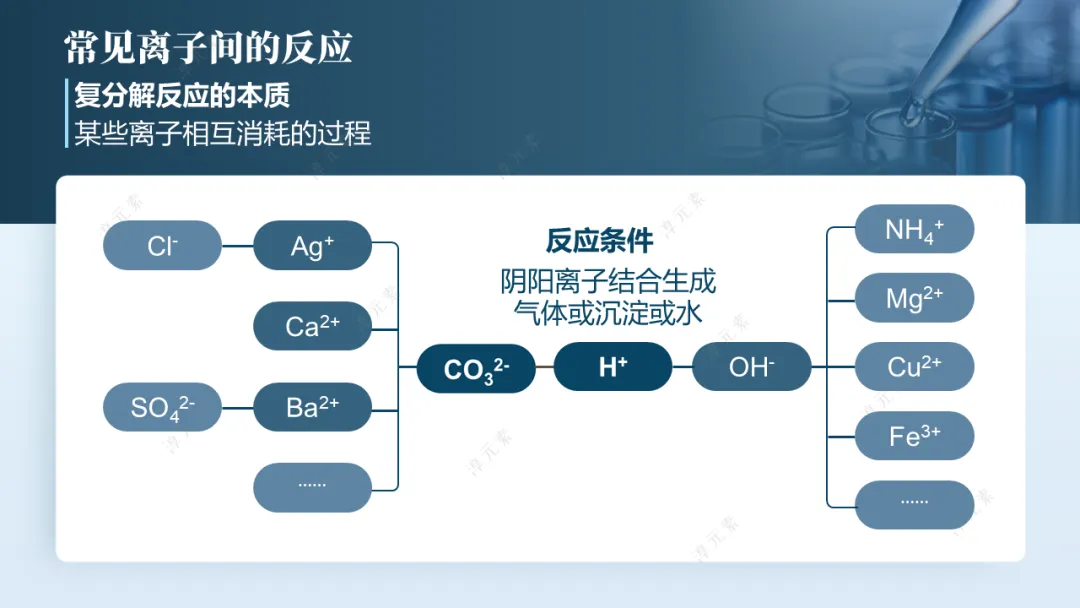
○归纳梳理:复分解反应的本质是某些离子相互消耗的过程,宏观条件为阴阳离子结合生成沉淀、气体或水,并结合PPT呈现离子反应网络图(CO32−、OH−、H+等的反应)。
(四)模块三:氧绽——爆炸盐,浣纱之智的化学创新(10分钟)
过渡语:“肥皂遇硬水会生成沉淀,去污能力大幅下降,为了解决这一问题,现代化学人创新研制出了新一代洗涤剂——爆炸盐,它遇水会产生大量气泡,去污漂白能力更强,这‘氧绽’的背后藏着怎样的化学原理?又有哪些使用技巧?”
1.新知铺垫:爆炸盐的成分与去污原理
○展示爆炸盐标签,介绍主要成分:过氧碳酸钠(2Na2CO3·3H2O2)。
○原理讲解:过氧碳酸钠遇水分解生成碳酸钠和过氧化氢,碳酸钠显碱性可去污,过氧化氢分解产生的活性氧具有漂白、除菌作用;“爆炸”是气泡剧烈翻滚的形象描述,并非真正的爆炸。
2.实验探究5:探究过氧化氢分解的促进因素
○提出问题:过氧化氢常温下分解速率较慢,为何爆炸盐加入温水后会产生大量气泡?过氧碳酸钠溶液中的哪种微粒对过氧化氢分解有促进作用?
○猜想假设:猜想一(CO32−)、猜想二(OH−)、猜想三(CO32−和OH−)。
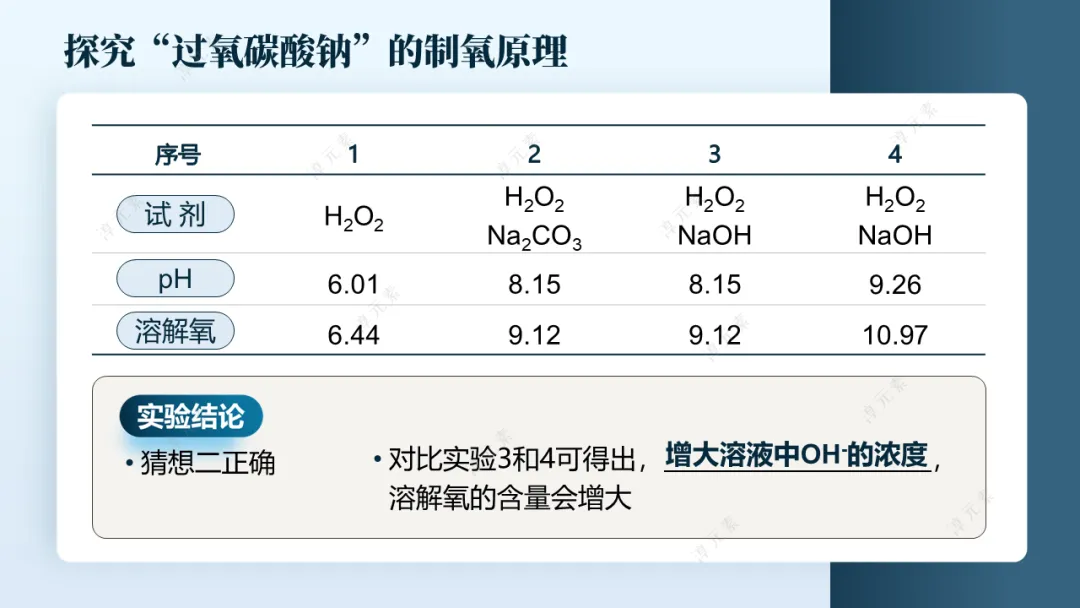
○对比实验:相同温度下,测定4%H2O2溶液、H2O2+Na2CO3、H2O2+NaOH、不同pH的H2O2+NaOH溶液的pH和溶解氧含量。
○数据分析:
① H2O2+Na2CO3与H2O2+NaOH的pH和溶解氧含量一致,排除猜想一、三,猜想二正确(OH−促进分解);
② 对比不同pH的NaOH组,pH越大(OH−浓度越高),溶解氧含量越大。
○得出结论:过氧碳酸钠溶液中的OH−对过氧化氢分解有促进作用,OH−浓度越高,分解速率越快。
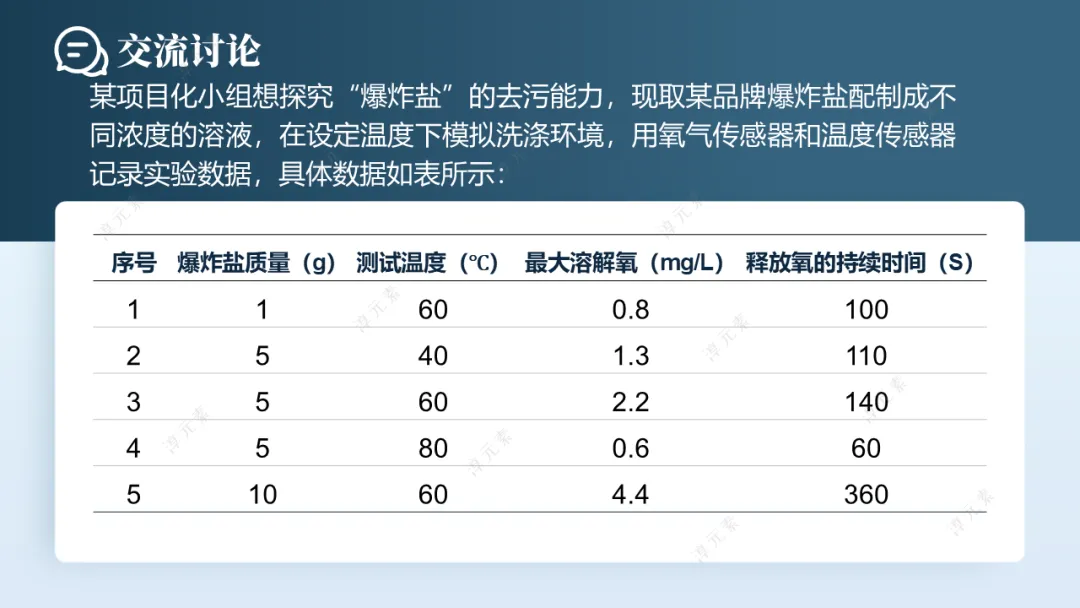
3.实验探究6:分析爆炸盐的去污能力与使用注意事项
○展示实验数据:不同质量、不同温度的爆炸盐溶液的最大溶解氧、释氧持续时间。
○小组讨论:
① 实验通过测量哪些数据衡量爆炸盐的去污能力?(最大溶解氧、释放氧的持续时间,氧含量越高、持续时间越长,去污漂白能力越强)
② 影响爆炸盐去污能力的因素有哪些?(爆炸盐的质量、温度)
③ 爆炸盐的使用注意事项有哪些?(避免与酸性物质混合使用,碳酸钠会与酸反应,酸性环境抑制过氧化氢分解;控制在60℃左右使用,温度过高过氧化氢分解过快,释氧时间短;控制合适浓度,并非浓度越高越好)
○拓展延伸:展示现代洗涤剂(洗衣凝珠、洗衣液、柔顺剂),说明化学创新始终围绕“提升去污能力、适配不同需求”展开,体现“创中学”的理念。
(五)课堂小结:梳网成络,融智于用(3分钟)
师生共同以洗涤剂演进为线索,梳理酸碱盐的知识网络,用思维导图呈现核心内容。

用匠心打造课件的每一页
把每一节课当做礼物送给学生



下面开始为加密文档
●19 绣球花的调色密码(酸碱复习)☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆
☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆☆
●……
新版人教版2.0和沪教版3.0新授课课件已经全部完稿,欢迎在公众号上面查看



工作微信号:pures2020(仅此一个工作微信,请勿上当受骗)
友情提醒:淳元素所创作的课件已有了版权,同行请勿随便盗版,在文件一些不易察觉的地方已经加了印记,需要的时候将作为法律证据。







