(点击查看详情)
中考生物知识点汇总
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈
中考化学考点汇总
备考指南


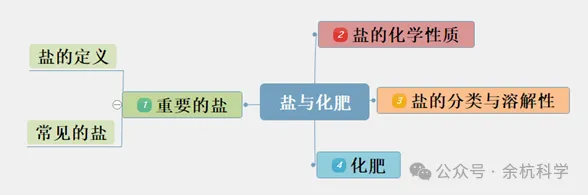
知识导图

考点梳理

考点一 盐的性质和应用

一、盐的定义与分类
1、盐的定义
由金属阳离子(或铵根离子)和酸根阴离子构成的化合物称为盐。盐是酸碱反应的产物之一。
2、盐的分类(盐的分类方法有很多,常见的分类方法有以下两种):
(1)按照盐带的离子分类
①正盐:NaCl、Na2CO3、CuSO4、NH4Cl
②酸式盐(带H+):NaHSO4
③碱式盐(带OH-):Cu2(OH)2CO3、Mg(OH)Cl
注意:盐中不一定含有金属阳离子,盐中可以含有H+或OH-<铜绿:Cu2(OH)2CO3>。
(2)按照盐的溶解性分类
①可溶性盐,常见的可溶性盐有K+、Na+、NH4+等离子与酸根离子形成的盐,如:碳酸钠(Na2CO3)、硫酸钾(K2SO4) 、硝酸银(AgNO3) 和氯化铵(NH4Cl)等。
②难溶性盐,常见的不溶性盐有硫酸盐中的BaSO4、盐酸盐中的AgCl和大部分的碳酸盐,如:硫酸钡(BaSO4)、氯化银(AgCl)、碳酸铜(CuCO3)、碳酸钙(CaCO3) 等。还有些盐是微溶于水的。
(3)盐的溶解性记忆口诀:
钾钠铵硝溶于水,盐酸盐除氯化银;硫酸盐除硫酸钡,碳酸盐溶钾钠铵;
微溶盐类有三种,硫酸钙银碳酸镁。
3、结晶水合物
(1)很多盐结晶时会带上结晶水,例如:CuSO4·5H2O
(2)风化:结晶水合物失去结晶水的过程叫风化。
①风化是一个化学反应。②用途:使用硫酸铜检验水。
二、几种盐的性质
1、碳酸钠(Na2CO3)
(1)俗名:纯碱、苏打。
(2)物理性质:白色粉末,易溶于水。
(3)化学性质
①水溶液显碱性,能使无色酚酞试液变红,使紫色石蕊试液变蓝。
②能和酸反应生成新盐和新酸(如:Na2CO3+2HCl=2NaCl+H2O+CO2↑,H2O和CO2是H2CO3分解的产物)。
③能和某些碱反应生成新盐和新碱(如:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH)。
④能和某些盐反应生成两种新盐(如:Na2CO3+BaCl2=2NaCl+BaCO3↓)
(4)用途:重要的化工原料,可用来制造玻璃、肥皂,去油污等。
2、碳酸氢钠(NaHCO3)
(1)白色固体,易溶于水,存在于天然碱湖,俗称小苏打,水溶液呈碱性。
碳酸氢钠+盐酸:NaHCO3+HCl===NaCl+H2O+CO2↑
(2)用途:在灭火器中,它是产生二氧化碳的原料之一;在食品工业上,它是的一种发酵粉主要原料;在医疗上,它是治疗胃酸过多的一种药剂。
3、碳酸钙(CaCO3)
(1)碳酸钙是一种难溶的盐,是碳酸(H2CO3)和氢氧化钙发生中和反应产物:Ca(OH)2+H2CO3== CaCO3↓+2H2O。存在:大理石、石灰石、汉白玉、鸡蛋壳等物质的主要成分都是碳酸钙。
(2)物理性质:白色固体,难溶于水。
(3)化学性质
①加强热能分解产生二氧化碳和生石灰( CaCO3=高温=CaO+CO2↑)。
②与酸反应生成新盐和新酸(如:CaCO3+2HC1 =CaCl2+H2O+CO2↑,H2O和CO2是H2CO3分解的产物)。
(4)用途:重要的建筑原料,可用来制水泥、炼钢、制生石灰等。
4、氯化钠(NaCl)
(1)俗名:食盐。
(2)物理性质:白色固体,易溶于水,有咸味。溶解度受外界温度变化影响不大。
(3)化学性质:能与某些盐反应生成两种新盐(NaCl+AgNO3=AgCl↓+NaNO3)。
(4)用途:重要的调味品,用来腌渍蔬菜;可用来制取烧碱、金属钠、氯气等;医疗上用氯化钠配制生理盐水(溶质质量分数为0.9%);浓的食盐溶液会使细胞内的水渗出,使蛋白质凝固,具有杀菌作用;农业上用定浓度的氯化钠溶液来选种等。
5、盐的制取
人们常利用一些盐的溶解性来实现盐的制取提纯和鉴别,盐的制取主要有以下几种方法。
(1)有些盐是天然存在的,通过物理方法提取,如可从海水盐湖或盐井中提取食盐。
(2)用化学方法制取
Na2CO3和CaCl2制取CaCO3和NaCl,反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl;
我国化学家侯德榜对制碱工业有重大贡献,他发明了“侯氏制碱法”,广泛应用于工业生产中,其原理为:NH3+CO2+H2O+NaCl == NaHCO3+NH4Cl、2NaHCO3△Na2CO3+H2O+CO2↑。
三、粗盐提纯
1、粗盐提纯目的:除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,得到纯净的NaCl。
2、原理:除Ca2+用CO32-,除Mg2+用OH-,除SO42-用Ba2+。
3、操作步骤:
(1)加过量BaCl2溶液;(2)加过量Na2CO3溶液;(3)过滤;(4)加适量HCl溶液。
4、加过量NaOH溶液,该步骤可穿插在(1)(2)步前后或之间的任意位置,BaCl2必须在Na2CO3之前加入。过滤和加适量HCl溶液的顺序不能变。
四、盐的通性
1、盐的化学性质
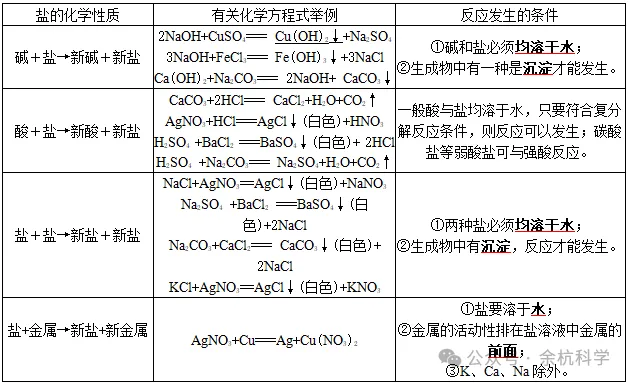
考点二 化学肥料

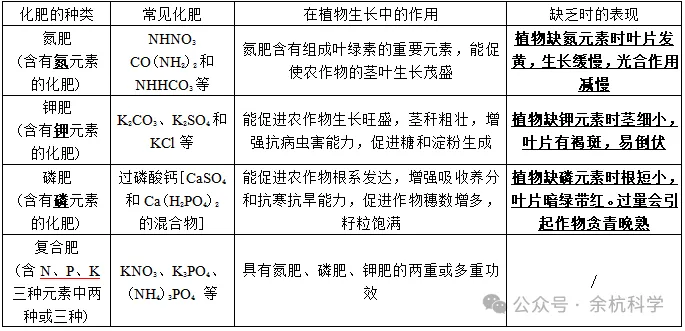
1、常见化肥的种类和作用
来自自然界的一些物质及一些人工合成的盐,它们能为农作物的生长提供养料,被称为化学肥料。
2、铵盐的制取
工业上用酸与氨气反应制氮肥(铵盐)
NH3+H2O+CO2 = NH4HCO3 (碳铵)
2NH3+H2SO4 = (NH4)2SO4 (硫铵)
3、合理使用化肥
虽然化肥有助于植物生长,但长期使用化肥往往使土壤板结,破坏土壤结构,因此通常需施一些农家肥料(有机肥),农家肥中含有大量有机物和多种营养元素,有利于改良土壤结构,提高土壤肥力。
【能力拓展】
(1)盐的组成中,所含的阳离子不一定都是金属阳离子,也可以是由多种元素的原子形成的复杂阳离子(带电原子团),如NH4+。
(2)我们把作氨肥的铵盐叫做铵态氨肥。铵盐能与碱反应,放出氨气,因此铵态氨肥不能与碱性的物质混合使用,否则会降低肥效。
(3)铵盐的检验
①原理:铵盐与碱混合(必要时加热),发生复分解反应,放出有刺激性气味的氨气,氨气是碱性气体,能使湿润的红色石蕊试纸变蓝,反应的化学方程式如下:
NH4HCO3+Ca(OH)2=CaCO3↓+2H2O+NH3↑,(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑。
②检验方法:取样品与碱溶液混合加热,放出有刺激性气味的气体,用湿润的红色石蕊试纸检验放出的气体,如果湿润的红色石蕊试纸变蓝,证明有铵根离子存在。
考点三 复分解反应

1、概念:两种化合物互相交换成分生成两种新化合物的反应(通式表示为AB+CD→AD+CB )。
2、特点:复分解反应交换成分,但反应前后各元素的化合价不变。
3、复分解反应发生的条件
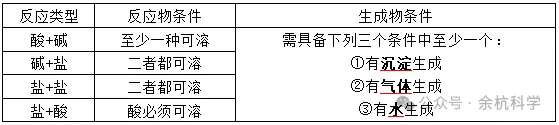
4、复分解反应实质:发生复分解反应的两种物质在水溶液中相互交换离子,结合成难电离的物质-沉淀、气体和水。