(点击查看详情)
中考生物知识点汇总
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈
中考化学考点汇总
备考指南

考点分布 | 考查频率 | 命题趋势 |
考点1常见的酸和碱 | ☆☆☆ | ①概述常见酸和碱的主要性质,学会用酸碱指示剂和pH试纸测定溶液的酸碱性 ②认识酸和碱反应的实质,举例说明酸碱反应在生产、生活中的应用 |
考点2酸碱指示剂、酸碱度、酸碱反应 | ☆☆ | |
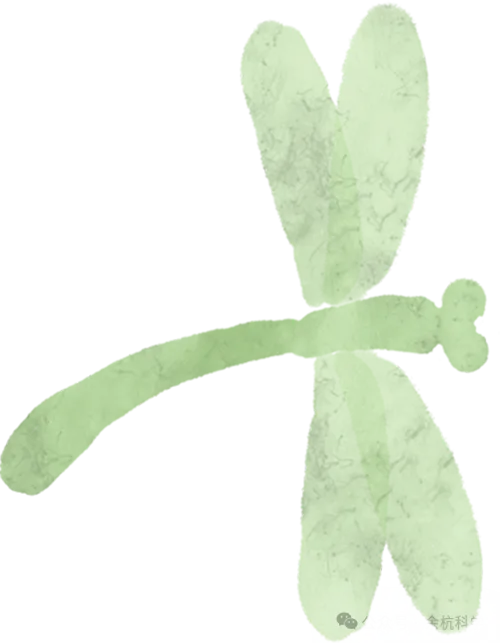
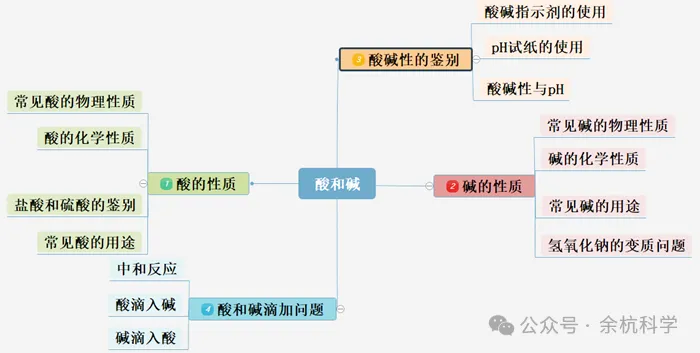
知识导图

考点梳理

考点一 常见的酸和碱

一、盐酸(HCl)
1、浓盐酸的物理性质
纯净的浓盐酸是无色的液体,有刺激性气味,具有挥发性(故需要密封保存)。打开瓶塞后能在空气中形成白雾。工业盐酸因含有Fe3+而呈黄色。
(1)浓盐酸具有挥发性,挥发出的氯化氢气体遇到空气中的水蒸气又形成盐酸的小液滴,故出现白雾现象。
(2)如果浓盐酸敞口放置,由于浓盐酸具有挥发性,挥发出溶质HCl,会导致溶液质量和溶质的质量分数都减小,故浓盐酸要密封保存。
2、稀盐酸的化学性质
化学性质 | 与其反应的物质 | 反应现象 | 化学方程式 |
与指示剂 作用 | 石蕊试液 酚酞试液 | 能使紫色的石蕊试液变红 不能使无色酚酞试液变色 | / |
与活泼金属反应 | 铁钉 | 有气泡产生,溶液由无色变为浅绿色 | Fe+2HCl = FeCl2+H2↑ |
与金属氧化物反应 | 生锈的铁钉(铁锈的主要成分Fe2O3) | 红棕色的铁锈逐渐溶解,溶液由无色变为黄色 | Fe2O3+6HCl = 2FeCl3+3H2O |
氧化铜 | 黑色的氧化铜粉末逐渐溶解,溶液由无色变为蓝色 | CuO+2HCl = CuCl2+H2O | |
与碱反应 | 氢氧化铜 | 蓝色的氢氧化铜逐渐溶解,溶液由无色变为蓝色 | Cu(OH)2+2HCl=CuCl2+2H2O |
与某些盐 反应 | 鸡蛋壳 (主要成分是碳酸钙) | 产生大量的气泡,生成的气体能使燃着的木条熄灭 | CaCO3+2HCl = CaCl2+H2O+CO2↑ |
硝酸银溶液 | 产生白色沉淀,滴加稀硝酸沉淀不溶解 | HCl+AgNO3 = AgC1↓+HNO3 |
二、硫酸(H2SO4)
1、浓硫酸
(1)浓硫酸是无色、黏稠、油状的液体,难挥发,密度比水大(物理性质)。
(2)浓硫酸具有以下特性
①强腐蚀性(化学性质):浓硫酸对皮肤、衣服等有强烈的腐蚀作用。如果浓硫酸不慎溅到皮肤上,要先用干布拭去,然后用大量清水冲洗,最后用小苏打溶液冲洗,严重时应立即送医院。O2、H2、CO2、SO2等气体可用浓硫酸进行干燥,但是能与其反应的NH3等碱性气体不可用它干燥。
②吸水性(物理性质):能直接吸收空气中的水分(故需要密封保存),所以常作为某些气体的干燥剂。
③脱水性(化学性质):能把由C、H、O等元素组成的化合物里的H、O元素按原子个数比2:1的比例从化合物中“脱出”结合成水,因而具有脱水性。
2、浓硫酸的稀释

由于浓硫酸溶于水时放出大量的热,因而在稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢地注人水里,并用玻璃棒不断搅拌,使产生的热量迅速扩散,切不可把水直接倒人浓硫酸中。
不可把水倒入浓硫酸中稀释的原因:水的密度比浓硫酸小,若把水倒入浓硫酸中,水浮在浓硫酸表面,浓硫酸溶于水时放出的热会使水立刻沸腾,使硫酸液滴向四周飞溅,造成危险。
3、稀硫酸的化学性质
化学性质 | 与其反应的物质 | 反应现象 | 化学方程式 |
与指示剂作用 | 石蕊试液 酚酞试液 | 能使紫色的石蕊试液变红, 不能使无色酚酞试液变色 | / |
与活泼金属反应 | 锌粒 | 有气泡产生 | Zn+H2SO4 = ZnSO4+H2↑ |
与金属氧化物 反应 | 生锈的铁钉(铁锈的主要成分Fe2O3 | 红棕色的铁锈逐渐溶解,溶液由无色变为黄色 | Fe2O3+3H2SO4 = Fe2(SO4)3+3H2O |
氧化铜 | 黑色的氧化铜粉末逐渐溶解,溶液由无色变为蓝色 | CuO+H2SO4 = CuSO4+H2O | |
与碱反应 | 氢氧化铜 | 蓝色的氢氧化铜逐渐溶解,溶液由无色变为蓝色 | Cu(OH)2+H2SO4 = CuSO4+2H2O |
与某些盐反应 | 碳酸钠 | 产生大量的气泡,生成的气体能使燃着的木条熄灭 | Na2CO3+H2SO4 = Na2SO4+H2O+CO2↑ |
氯化钡溶液 | 产生白色沉淀,滴加稀硝酸沉淀不溶解 | BaCl2+H2SO4 = BaSO4↓+2HCl |
三、盐酸与硫酸的用途比较
酸 | 用途 |
盐酸(HCl) | 重要化工产品,用于金属表面除锈、制造药物(如盐酸麻黄素氯化锌)等; 人体胃液中含有盐酸,可帮助消化。 |
硫酸(H2SO4) | 重要化工原料,用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。浓硫酸有吸水性,在实验室中常用它做干燥剂。 |
四、硝酸
1、物理性质:无色、有刺激性气味,液体,易挥发;能在空气中形成硝酸小液滴而成白雾。
2、化学性质:也有类似盐酸的化学性质。
3、浓硝酸的特性:强氧化性,与金属反应不产生H2,而是水,能强烈腐蚀衣服和皮肤,使用时小心。【了解】
五、酸的通性
1、酸的通性
酸的通性 | 反应情况 | 化学方程式 |
与指示剂作用 | 能使紫色的石蕊试液变红 不能使无色酚酞试液变色 | / |
与活泼金属反应 | 生成盐和氢气 | Zn+H2SO4 = ZnSO4+H2↑ Fe+2HCl = FeCl2+H2↑ |
与金属氧化物反应 | 生成盐和水 | Fe2O3+3H2SO4 = Fe2(SO4)3+3H2O Fe2O3+6HCl = 2FeCl3+3H2O CuO+H2SO4 = CuSO4+H2O CuO+2HCl = CuCl2+H2O |
与碱反应 | 生成盐和水 | Cu(OH)2+H2SO4 = CuSO4+2H2O Mg(OH)2+2HCl=MgCl2+2H2O |
与某些盐反应 | 生成新盐和新酸 | Na2CO3+H2SO4 = Na2SO4+H2O+CO2↑ HCl+AgNO3 = AgC1↓+HNO3 BaCl2+H2SO4 = BaSO4↓+2HCl |
2、酸具有相似化学性质的原因
①酸的电离实质:溶于水后电离出的阳离子全部是氢离子,阴离子是酸根离子。
②相同点:不同的酸都能电离出H+。
③不同点:不同的酸电离出的酸根阴离子不同。
④酸具有相似化学性质的原因:酸在水中都电离出相同的阳离子——H+。
六、Cl-和SO42、CO32-三种离子的检验
1、Cl- :先向待测液中滴加AgNO3溶液,出现白色沉淀后再滴加稀HNO3,沉淀不消失。相关的化学方程式:HCl+AgNO3=AgCl↓+HNO3(以HCl为例)。
2、SO42- :先向待测液中滴加Ba(NO3)2溶液,出现白色沉淀后再滴加稀HNO3,沉淀不消失。相关的化学方程式:H2SO4+Ba(NO3)2=BaSO4↓+2HNO3(以H2SO4为例)。
3、CO32- :加盐酸,能产生使澄清石灰水变浑浊的气体(二氧化碳)。
相关化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O。
注:检验Cl-和SO42-时,要加几滴稀硝酸,目的是除去CO32—等杂质离子的干扰。
因为CO32—与AgNO3或BaCl2溶液接触时,也有白色沉淀Ag2CO3、BaCO3生成,但这些沉淀都溶于稀硝酸。溶液有可能同时存在Cl-和SO42-时,应该先检验SO42-,而且用Ba(NO3)2溶液和稀硝酸代替BaCl2溶液和盐酸作试剂。且需将BaSO4沉淀滤去,再往滤液中加AgNO3溶液和稀硝酸检验Cl-。 因为硫酸银微溶于水,如果溶液中SO42-浓度较大,先检验Cl-,加入AgNO3溶液时,会生成Ag2SO4(微溶)沉淀,而干扰Cl-的检验。
七、氢氧化钠( NaOH )
1、俗名:烧碱、火碱、苛性钠。
2、物理性质:常态下为白色固体,易潮解(暴露在空气中容易吸收空气中的水分,表面潮湿而逐步溶解),极易溶于水且放出大量的热,水溶液有滑腻感、有涩味。
3、化学性质:具有较强的腐蚀性,能腐蚀兔毛或全毛绒线;具有碱的通性。不能放在纸片上称量,应放在烧杯等玻璃器皿中称量。
4、变质:氢氧化钠易与空气中的二氧化碳发生反应而变质,变质生成碳酸钠,化学反应方程式:2NaOH+CO2 =Na2CO3 + H2O。
5、用途:重要的化工原料,应用于造纸制铝、制皂精炼石油等工业;生活中可用来除油污等。
八、氢氧化钙[Ca(OH)2 ]
1、俗名:熟石灰、消石灰。
2、物理性质:常态下为白色粉末状固体,微溶于水(溶解度随温度的升高而减小)。
3、化学性质:
(1)具有较强的腐蚀性。
(2)能与CO2、SO2等反应,如CO2+Ca(OH)2 = CaCO3↓+H2O,这一反应常用于检验CO2。
(3)能与酸反应,反应过程无明显现象,如Ca(OH)2与HCl和H2SO4的反应如下:
Ca(OH)2+2HCl = CaCl2+2H2O;Ca(OH)2+H2SO4= CaSO4+2H2O。
(4)能与部分盐反应,生成沉淀:
2FeCl3+3Ca(OH)2 = 2Fe(OH)3↓+3CaCl2;Ca(OH)2+Na2CO3 = CaCO3↓+2NaOH。
Fe(OH)3为红褐色沉淀,CaCO3为白色沉淀。
4、用途:重要的建筑材料,也是一种工业原料。如用来制取漂白粉,农业上用于改良酸性土壤等。
5、Ca(OH)2的制取:将生石灰(CaO)溶于水(剧烈反应、放出大量的热),发生反应的化学方程式为CaO+H2O = Ca(OH)2。
九、碱的通性
1、碱的通性
碱的通性 | 反应情况 | 示例 |
能使指示剂变色 | 能使紫色石蕊试液变蓝 能使无色酚酞试液变红 | NaOH、Ca(OH)2等可溶性碱均能使紫色石蕊试液变蓝 使无色酚酞试液变红。 |
能与某些非金属氧化物反应 | 生成盐和水 | 2NaOH+SO2 = Na2SO3 (亚硫酸钠)+H2O 氢氧化钠溶液来吸收二氧化硫; Ca(OH)2 +CO2 = CaCO3↓+H2 O 可用来检验二氧化碳的存在; 2NaOH+CO2 = Na2CO3+H2O 常用来吸收二氧化碳; 2NaOH+SiO2 = Na2SiO3+H2O 盛放NaOH溶液的试剂瓶不能用玻璃塞,应用橡皮塞或木塞。 |
能与酸反应 | 生成盐和水 | NaOH+HCl = NaCl+H2O Ca(OH)2+2HCl = CaCl2+2H2O |
能与某些盐反应 | 生成新盐和新碱 | 3NaOH+FeCl3 = Fe(OH)3↓+3NaCl Ca(OH)2+Na2CO3= CaCO3↓+2NaOH |
2、常见的不溶性碱有:Mg(OH)2、Al(OH)3、Zn(OH)2、Fe(OH)3、Cu(OH)2,它们不能使加入的指示剂变色。Mg(OH)2、Al(OH)3、Zn(OH)2是白色沉淀,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色絮状沉淀。
考点二 酸碱指示剂、酸碱度、酸碱反应

一、酸性物质和碱性物质
1、电离
(1)概念:物质溶解于水或受热熔化而形成自由移动离子的过程。在溶液里,所有的阳离子带的正电荷总数和所有阴离子带的负电荷总数相等,溶液不显电性。
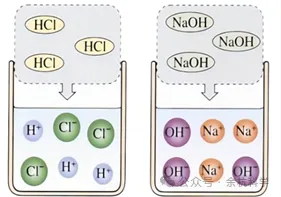
(2)电离方程式:用化学式和离子符号来表示物质电离的式子。书写时,等号左边是物质的化学式,右边是构成物质的离子的符号。如:NaCl溶于水的电离方程式为NaCl==Na++Cl-。
<书写电离方程式时,应注意以下几点:(1)不必写条件;(2)配平,使正、负电荷数相等;(3)原子团不能拆开书写>。
2、酸
(1)概念:电离时生成的阳离子都是氢离子(H+)的化合物。
某种酸电离产生的阴离子叫做这种酸的酸根离子,如SO42-是H2SO4的酸根。其他常见酸根有CO32-、NO3-、Cl-。
(2)常见酸的电离方程式:H2SO4==2H++SO42-;HC1==H++Cl-;HNO3==H++NO3-
(3)生活中常见的酸:盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3)、碳酸(H2CO3)、醋酸(CH3COOH)等。
3、碱
(1)概念:电离时生成的阴离子都是氢氧根离子(OH-)的化合物。
(2)常见碱的电离方程式:NaOH==Na++OH-;Ca(OH)2==Ca2++2OH-; KOH==K++OH-。
(3)生活中常见的碱:氢氧化钠、氢氧化钙、氢氧化钾、氢氧化钡、氨水(NH3的水溶液)等。能电离出H+ 的不一定是酸,能电离出OH- 的不一定是碱。
二、酸碱指示剂
1、酸碱指示剂
在酸性或碱性溶液里能显示出不同颜色的物质,叫做酸碱指示剂,通常简称指示剂。
2、常用的酸碱指示剂在酸性和碱性溶液中的变色情况
指示剂 | 酸性溶液 | 碱性溶液 |
石蕊试液(紫色) | 变红色 | 变蓝色 |
酚酞试液(无色) | 不变色 | 变红色 |
蓝色石蕊试纸 | 变红色 | 不变色 |
红色石蕊试纸 | 不变色 | 变蓝色 |
紫色石蕊遇酸变红色,遇碱变蓝色;无色酚酞遇酸不变色,遇碱变红色(指溶液,不特指酸碱)
不溶于水的酸和碱,不能使指示剂变色;指示剂变色的过程是化学变化。
3、自制酸碱指示剂
许多植物的花、果茎、叶中都含有某些显色的物质,它们在酸性溶液或碱性溶液里会显示不同的颜色。如果你有兴趣,可以取这些植物的花果茎、叶切碎捣烂,用酒精浸制,所得的浸出液可以作为酸碱指示剂。
三、溶液酸碱性的强弱程度
1、溶液的酸碱度
不同酸溶液的酸性强弱不同,不同碱溶液的碱性强弱也不同。酸碱指示剂只能测量溶液的酸碱性,无法衡量酸碱性强弱的程度。用酸度、碱度来表示溶液酸性或碱性强弱的程度。
(1)pH:用来表示溶液酸碱性的强弱程度。
(2)取值范围通常:0~14。
(3)溶液酸碱性的强弱程度与pH的关系如图所示。
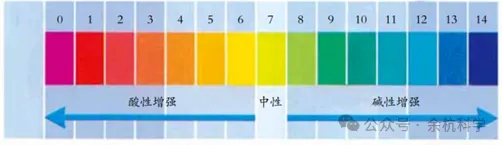

2、测定溶液pH的方法
(1)测定溶液酸碱性强弱最常用、最简单的方法是使用pH试纸。
(2)pH的测定方法:用干燥洁净的玻璃棒蘸取被测试的溶液,滴在pH试纸上,将试纸显示的颜色与标准比色卡对照,看与哪种颜色最接近,从而确定被测溶液的pH。根据pH便可判断溶液的酸碱性强弱。
注意:
(1)用pH试纸测溶液pH时,pH试纸不能预先用蒸馏水润湿,否则会导致测量结果不准确,常见的情况如下:
①溶液为酸性时,酸性变弱,pH偏大。
②溶液为中性时,pH不变。
③溶液为碱性时,碱性变弱,pH偏小。
(2)不能将pH试纸直接放入待测试的溶液中,否则会污染试剂。
四、溶液酸碱性与生命活动的关系
1、人体胃液的正常pH为0.9~1.5;人体血液的pH为7.35~7.45。【与人体的关系】
2、人的汗液的pH为5.5~6.6;食醋里含有醋酸,它的pH为3左右;牛奶的pH通常小于7;酱油的pH为4.8左右;番茄的pH≤4.5;生鲜肉的pH为7.0~7.4。【与生活的关系】
3、土壤的酸碱性的强弱对农作物生长有很大的影响,各种农作物对pH有一定的适应性。【与土壤的关系】
4、雨水因溶有空气中的二氧化碳而略显酸性,正常雨水的pH≈5.6。某些地区因工业生产产生的酸性气体(二氧化硫、氮的氧化物等)直接向空气中排放而导致雨水的酸性增强。通常把pH小于5.6的降水称为酸雨。【与环境的关系】
五、酸碱反应
1、酸碱反应实验
向盛有氢氧化钠的烧杯中滴入几滴酚酞试液,溶液变红,向变红的溶液中滴加稀盐酸(或稀硫酸),边滴边振荡,溶液颜色变浅直至消失,说明溶液由碱性变为中性或酸性,碱和酸发生了反应。
2、实验过程中溶液中溶质、pH以及颜色的变化
反应进程 | 溶质 | PH | 颜色 |
未滴加稀盐酸 | NaOH | pH>7 | 红色 |
滴加少量稀盐酸(氢氧化钠过量) | NaOH + NaCl | pH>7 | 红色 |
滴加适量稀盐酸(恰好完全反应) | NaCl | pH=7 | 无色(红色刚好褪去) |
滴加过量稀盐酸 | NaCl + HCl | pH<7 | 无色 |
◆酸碱反应时pH的变化曲线【“蛇线”图】
注:酸碱互滴图像,溶液的酸碱性也发生改变,最终都无限接近某一个值
类型 | pH变化过程 | 溶质成分 | 图象 |
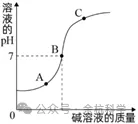
碱 入 酸 | 开始时,溶液的pH<7,溶液呈酸性; 随着碱的加入,pH逐渐增大; 当酸碱恰好完全反应时, 溶液的pH=7,溶液呈中性; 随着碱的继续加入,溶液的pH>7, 溶液呈碱性 | A:HCl B:NaCl C:NaCl、NaOH |
|
类型 | pH变化过程 | 溶质成分 | 图象 |
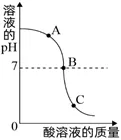
酸 入 碱 | 开始时,溶液的pH>7,溶液呈碱性;随着碱的加入,pH逐渐减小; 当酸碱恰好完全反应时, 溶液的pH=7,溶液呈中性; 随着酸的继续加入,溶液的pH<7, 溶液呈酸性 | A:NaOH B:NaCl C:NaCl、HCl |
|
(1)酸、碱反应实验选用的指示剂是酚酞溶液。如果使用石蕊溶液,溶液由蓝色变为紫色,颜色变化不明显。
(2)实验时用玻璃棒不断搅拌,可以使稀盐酸和氢氧化钠溶液充分接触,反应迅速、完全。
(3)实验时用胶头滴管慢慢滴入,便于控制加入酸的量,同时也为了清楚地看出指示剂颜色的变化,当溶液由红色恰好变为无色时,应立即停止滴加,防止盐酸过量。
2、酸碱反应原理:酸和碱之间发生反应能生成盐和水。
如:HCl+NaOH = NaCl+H2O,H2SO4+2NaOH = Na2SO4+2H2O
3、酸碱反应的实质
(1)酸中的H+和碱中的OH-结合生成水,即H+ + OH- = H2O。
(2)特点:反应放热。
注意:
①有盐和水生成的反应不一定是酸碱反应,如金属氧化物与酸反应、非金属氧化物与碱反应均生成盐和水,但都不是酸碱反应。
②酸碱反应一定属于复分解反应,但复分解反应不一定是酸碱反应。
六、酸碱(中和)反应的应用
1、酸碱反应在农业生产中的应用
植物适宜在接近中性(pH在6.5~7.5)的土壤里生长,利用酸碱反应的原理,在酸(碱)性土壤中加人适量的碱(酸),调节土壤的酸碱性。如:农业上常施加熟石灰[主要含Ca(OH)2]来降低土壤的酸性。
注意:改良酸性土壤常使用熟石灰,而不使用碱性、腐蚀性很强的氢氧化钠。
2、酸碱反应在工业生产中的应用
(1)处理工业废水,解决环保问题。
(2)精制石油时,可用氢氧化钠来中和过量的酸。
3、酸碱反应在医药方面的应用