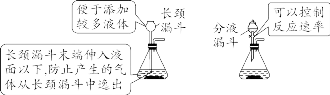
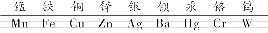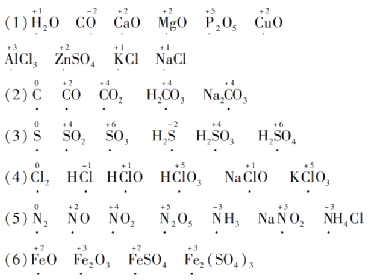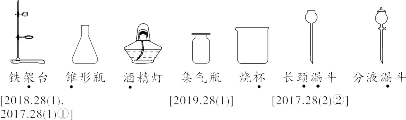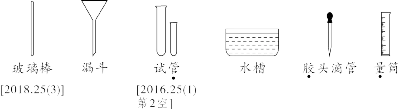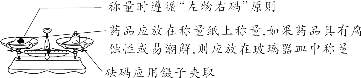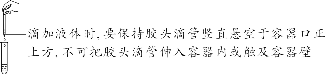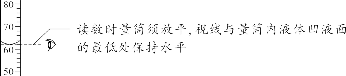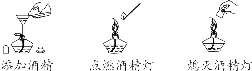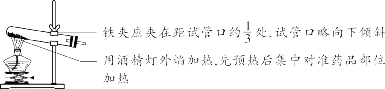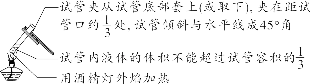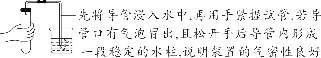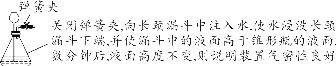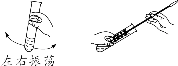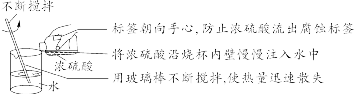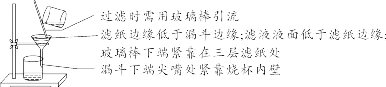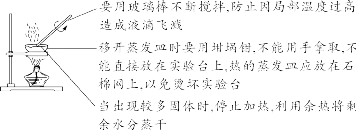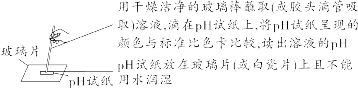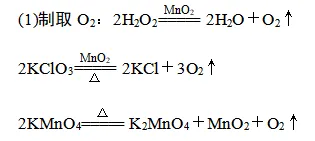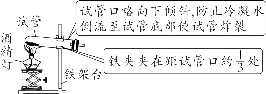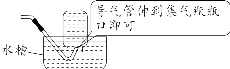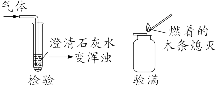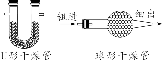中考化学方程式+高频考点六大块 备考速记
四季读书网
16
中考化学方程式+高频考点六大块 备考速记
【注意事项】书写元素符号时,元素符号由一个字母表示的必须大写,由两个字母表示的第一个必须大写,第二个必须小写。氢离子:H+ 钠离子:Na+ 钾离子:K+ 钙离子:Ca2+镁离子:Mg2+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+硅:Si 磷:P 硫:S 碘:I2 碳:C 硼:B氧化镁:MgO 氧化铜:CuO 氧化汞:HgO 氧化钙:CaO氧化铝:Al2O3 二氧化锰:MnO2 氧化铁:Fe2O3 四氧化三铁:Fe3O4二氧化氮:NO2 二氧化硫:SO2 五氧化二磷:P2O5盐酸:HCl 硫酸:H2SO4 硝酸:HNO3 碳酸:H2CO3氢氧化钠:NaOH 氢氧化钙:Ca(OH)2 氢氧化钾:KOH氢氧化镁:Mg(OH)2 氢氧化铜:Cu(OH)2 氢氧化铁:Fe(OH)3氯化钠:NaCl 氯化钾:KCl 氯化银:AgCl氯化铵:NH4Cl 氯化钙:CaCl2 氯化钡:BaCl2氯化铜:CuCl2 氯化亚铁:FeCl2 氯化铁:FeCl3硫酸钠:Na2SO4 硫酸钡:BaSO4 硫酸铜:CuSO4碳酸钠:Na2CO3 碳酸钙:CaCO3 碳酸钾:K2CO3硝酸银:AgNO3 硝酸钡:Ba(NO3)2 硝酸铵:NH4NO3b.表示物质的元素组成(表示乙醇是由碳、氢、氧三种元素组成的)微观意义:a.表示该物质的一个分子(表示一个乙醇分子)b.表示该物质一个分子的构成 [表示一个乙醇分子由9个原子(或2个碳原子、6个氢原子和1个氧原子)构成]微观意义:表示该物质的一个原子 (表示一个铁原子)C2H5OH的相对分子质量为12×2+1×6+16×1=46C2H5OH中碳、氢、氧三种元素的原子个数比为2∶6∶1C2H5OH中,mC:mH:mO=(12×2)∶(1×6)∶(16×1)=12∶3∶8如100 g C2H5OH中碳元素的质量=100 g×52.2%=52.2 g②M为化学式,除由原子直接构成的物质外,一般表示n个M分子(2)下角标数字的含义:表示一个分子中含有该原子的个数如:H2O中的“2”表示1个水分子中含有2个氢原子;P2O5中的“5”表示1个五氧化二磷分子中含有5个氧原子。(3)符号右上角数字的含义:表示离子或原子团所带的电荷数如:Fe2+中的“2”表示1个亚铁离子带2个单位的正电荷;S2-中的“2”表示1个硫离子带2个单位的负电荷;CO32-中的“2”表示1个碳酸根离子带2个单位的负电荷。(4)符号正上方数字的含义:表示某元素在该微粒中所显的化合价 | |
| 不能用手接触药品;不要将鼻孔直接凑到容器口闻药品的气味;不得尝任何药品的味道 |
| 严格按照实验规定的用量取用药品。如果没有说明用量,一般应该按最少量取用,液体取用量为1~2 mL,固体取用量为盖满试管底部即可 |
| 实验剩余药品既不能放回原试剂瓶中,也不要随意丢弃,更不要拿出实验室,要放到指定容器内 |
【特别提醒】①托盘天平的称量值只能精确到小数点后一位;若称量时药品与砝码位置放反且使用了游码,则药品的实际质量=砝码质量-游码读数。②称量一定质量的固体时,天平指针偏右,接下来的操作是继续加固体至天平平衡;称量某物质的质量时,天平指针偏左,接下来的操作是加砝码或移动游码。【注意事项】①取液后的胶头滴管应保持橡胶胶帽在上,不要平放或倒放,防止液体倒流,污染试剂或腐蚀橡胶胶帽;②用过的胶头滴管要立即用清水冲洗干净(滴瓶上的滴管不用冲洗),严禁用未经清洗的胶头滴管再吸取其他试剂。【注意事项】①量筒的选择:a.选择比量取液体体积稍大的量筒,且越接近越好,减少误差;b.保证只量取一次;②量筒不能用作反应容器或配制溶液的容器。 【注意事项】①绝对禁止向燃着的酒精灯里添加酒精,以免引起失火;②绝对禁止用燃着的酒精灯引燃另一只酒精灯;③用完酒精灯后,必须用灯帽盖灭,不可用嘴吹灭。【补充】可能导致试管炸裂的操作有:①加热完药品的试管,立即用冷水冲洗;②加热液体药品时,用酒精灯直接对准药品部位进行加热;③加热药品前,没有擦干试管外壁的水。【特别提醒】检查装置的气密性一般在组装仪器之后,装入药品之前。【特别提醒】刷洗时须转动或上下移动试管刷,但不能用力过猛,以防损坏试管。洗净的标准:洗过的仪器内壁附着的水既不聚成水滴,也不成股流下时,表明仪器已洗干净。【注意事项】若两次过滤后滤液仍然浑浊,原因可能是滤纸破损或过滤时漏斗内液面高于滤纸边缘等。②主要仪器:蒸发皿、酒精灯、玻璃棒、铁架台、坩埚钳【特别提醒】若要测定固体物质的酸碱性,应先取适量固体物质于烧杯中,加蒸馏水、搅拌、静置得到其饱和溶液,然后用测定溶液pH的方法进行测定。 | |
| |
| 浓酸:用大量水冲洗,涂3%~5%的NaHCO3溶液 |
| 立即用大量水冲洗,必要时请医生治疗,切不可用手揉眼睛 |
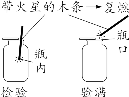
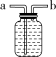
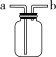
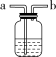
【巧记】谁含“Mn”不加“MnO2”,不含“Mn”加“MnO2”;固体要“加热”,液体“不加热”。(2)制取CO2:CaCO3+2HCl=== CaCl2+H2O+CO2↑【注意事项】用KMnO4制取氧气时,试管口要塞一团棉花,以防止加热时高锰酸钾粉末随氧气流进入导管,堵塞导管。举例:实验室用大理石或石灰石与稀盐酸反应制CO2;用双氧水制O2。(1)排空气法:操作简单,收集到的气体比较干燥但纯度不高。 适用范围 ①无毒无害,不与空气中各成分发生反应,且密度与空气密度相差 较大的气体 ②密度比空气大的气体(如O2、CO2),用向上排空气法(如图1) ③密度比空气小的气体(如H2、NH3),用向下排空气法(如图2)(2)排水法:难溶或不易溶于水,且不与水反应的气体,排水法收集的气体纯度较高,但含有一定量的水蒸气。【注意事项】a.排水法收集氧气的最佳时机:当导管口有气泡连续均匀冒出时开始收集;b.用加热装置制取气体时,实验结束后要先从水槽中取出导管再熄灭酒精灯,以防止水倒流造成试管炸裂;c.用排水法收集氧气时,观察到有大气泡从瓶口冒出,应该在水面下用玻璃片盖住瓶口,把集气瓶移出水槽,再将集满氧气的集气瓶正放在桌面上。 | |
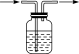
| a.当装有浓硫酸时,用于除去气体中的水分(或干燥气体),如:H2、CH4、N2、SO2、HCl、CO2等中性或酸性气体b.当装有NaOH溶液时,用于除去气体中的CO2、SO2、HCl等酸性杂质气体c.当装有饱和NaHCO3溶液时,用于除去CO2中的HCl |
| a.当装有碱石灰时,用于干燥碱性或中性气体(如H2、O2、N2、CH4、NH3等)、除去CO2、SO2等酸性气体b.当装有无水CaCl2时,用于干燥气体(NH3除外) |
①黑色:铁粉、炭粉(C)、CuO、MnO2、Fe3O4②红色:Fe2O3(或红棕色)、Cu(或紫红色)、红磷①蓝色⇔含Cu2+的溶液,如:CuSO4、Cu(NO3)2等溶液②浅绿色⇔含Fe2+的溶液,如:FeCl2、FeSO4等溶液③黄色⇔含Fe3+的溶液,如:FeCl3、Fe(NO3)3、Fe2(SO4)3等溶液②白色沉淀(5种):BaSO4、AgCl、CaCO3、BaCO3、Mg(OH)2【注意】不溶于稀硝酸的白色沉淀(2种):BaSO4、AgCl溶于酸并有气体放出的白色沉淀(2种):CaCO3、BaCO3溶于酸但没有气体放出的白色沉淀(1种):Mg(OH)2①能供给呼吸、支持燃烧、能使带火星木条复燃的气体是O2。【补充】具有吸附性,可用于净水、能除去冰箱中异味的是活性炭(主要成分为碳单质)。①可用作光合作用的原料、常用作灭火剂、制作汽水、固态可用于人工降雨的是CO2。②会导致温室效应,能使澄清石灰水变浑浊的气体是CO2。(2015.25)③具有还原性,可用于冶炼金属的气体是CO。(2014.25)④可作燃料且极易与血液中血红蛋白结合的有毒气体是CO。⑤与水具有相同元素组成且有消毒杀菌作用的液体是H2O2。①常用于金属表面除锈的物质是稀盐酸(HCl)、稀硫酸(H2SO4)。(2018.27)④常用来改良酸性土壤的是熟石灰[Ca(OH)2]。⑤实验室用来检验二氧化碳的试剂是澄清石灰水[Ca(OH)2]。⑩工业上广泛用于玻璃、造纸、纺织和洗涤剂生产的是Na2CO3。⑬用于配制波尔多液的是Ca(OH)2和CuSO4。⑭用于治疗胃酸过多的是Al(OH)3、Mg(OH)2、NaHCO3。①日常生活中应用最广泛的金属、目前世界上年产量最高的金属、提取量最大的金属:Fe④最理想的清洁燃料、相对分子质量最小的单质、密度最小的气体:H2(2)盐:FeCl2和FeCl3、FeSO4和 Fe2(SO4)3等①Fe⇐⇒Fe、Fe2O3、Fe3O4、FeCl3[或Fe2(SO4)3]、FeCl2(或FeSO4)、Fe(OH)3②Cu⇐⇒Cu、CuO、Cu(OH)2、CuCl2(或CuSO4)④Na⇐⇒NaCl、NaOH、Na2CO3、NaHCO3现象:在空气中燃烧发出微弱的淡蓝色火焰,在氧气中燃烧发出明亮的蓝紫色火焰;相同点:放出热量,生成有刺激性气味的气体。13. 二氧化碳与澄清石灰水[Ca(OH)2溶液]反应CO2+Ca(OH)2=== CaCO3↓+H2O15. 二氧化碳与水反应(使紫色石蕊溶液变红的原因):Zn+2HCl=== ZnCl2+H2↑现象:有气泡产生。19. 镁与稀硫酸反应Mg+H2SO4=== MgSO4+H2↑条件:①金属单质的活动性排在盐溶液中金属之前(K、Ca、Na除外);21. 铜与硝酸银溶液反应Cu+2AgNO3=== Cu(NO3)2+2Ag22. 锌与硫酸铜反应:Zn+CuSO4=== ZnSO4+Cu23. 铝与硫酸亚铁反应:2Al+3FeSO4=== Al2(SO4)3+3Fe24. 氧化铁与酸(稀盐酸、稀硫酸)反应(除铁锈)Fe2O3+6HCl=== 2FeCl3+3H2OFe2O3+3H2SO4=== Fe2(SO4)3+3H2O26. 稀盐酸与氢氧化钠反应:HCl+NaOH=== NaCl+H2O27. 稀硫酸与氢氧化铜反应:H2SO4+Cu(OH)2=== CuSO4+2H2O28. 稀盐酸与氢氧化钙反应:2HCl+Ca(OH)2=== CaCl2+2H2O29. 稀盐酸与氢氧化镁反应:2HCl+Mg(OH)2=== MgCl2+2H2O30. 稀硫酸与氢氧化钡反应:H2SO4+Ba(OH)2=== BaSO4↓+2H2O稀硫酸与氢氧化钠反应:H2SO4+2NaOH===Na2SO4+H2O稀硫酸与氢氧化钾反应:H2SO4+2KOH===K2SO4+H2OH2SO4+BaCl2=== BaSO4↓+2HCl2HCl+Na2CO3=== 2NaCl+CO2↑+H2O34. 稀硫酸与碳酸钠反应:H2SO4+Na2CO3=== Na2SO4+H2O+CO2↑HCl+2NaHCO3===Na2CO3+HCl+CO2↑Ca(OH)2+Na2CO3=== CaCO3↓+2NaOH2NaOH+CuSO4=== Na2SO4+Cu(OH)2↓2NaOH+CuCl2=== Cu(OH)2↓+2NaCl37. 氢氧化钠与氯化铁反应:3NaOH+FeCl3=== Fe(OH)3↓+3NaCl38. 氢氧化钡与硫酸钠反应:Ba(OH)2+Na2SO4=== BaSO4↓+2NaOHNa2CO3+CaCl2=== CaCO3↓+2NaCl40. 碳酸钠与氯化钡反应:Na2CO3+BaCl2=== BaCO3↓+2NaCl41. 氯化钠与硝酸银反应:NaCl+AgNO3=== AgCl↓+NaNO342. 硫酸钠与氯化钡反应:Na2SO4+BaCl2=== BaSO4↓+2NaCl▍来源:网络。本公众号尊重原创,好的内容值得分享,如有不妥请联系我们。本文图片均来自网络 联系QQ:3555406796
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至23467321@qq.com举报,一经查实,本站将立刻删除;如已特别标注为本站原创文章的,转载时请以链接形式注明文章出处,谢谢!