








【任务单1】小组一起欣赏“蓝色妖姬——硫酸铜晶体玫瑰花”。
问题1:如何制作“蓝色妖姬”呢?
问题2:硫酸铜溶液中溶质是什么?溶剂是什么?
问题3:从无水硫酸铜溶解度表中你能获得什么信息?10℃时,无水硫酸铜的溶解度是17.4g有什么含义?
【观察并思考】观察桌上的“蓝色妖姬”,并思考“任务单1”中的问题。
【生1】“蓝色妖姬”是通过硫酸铜溶液结晶得来的。
【生2】硫酸铜溶液中溶质是硫酸铜,溶剂是水。
【生3】从无水硫酸铜溶解度表中可以得到0℃、10℃、30℃、50℃和70℃时无水硫酸铜溶解度分别是14.3g、18.6g、24.2g、33.3g和46.8g。
【追问】10℃时,无水硫酸铜溶解度是18.6g有什么含义?
【生3】在10℃时,100g水中最多溶解18.6g无水硫酸铜。
【生4】在10℃时,18.6g无水硫酸铜溶解在100g水中形成饱和溶液。
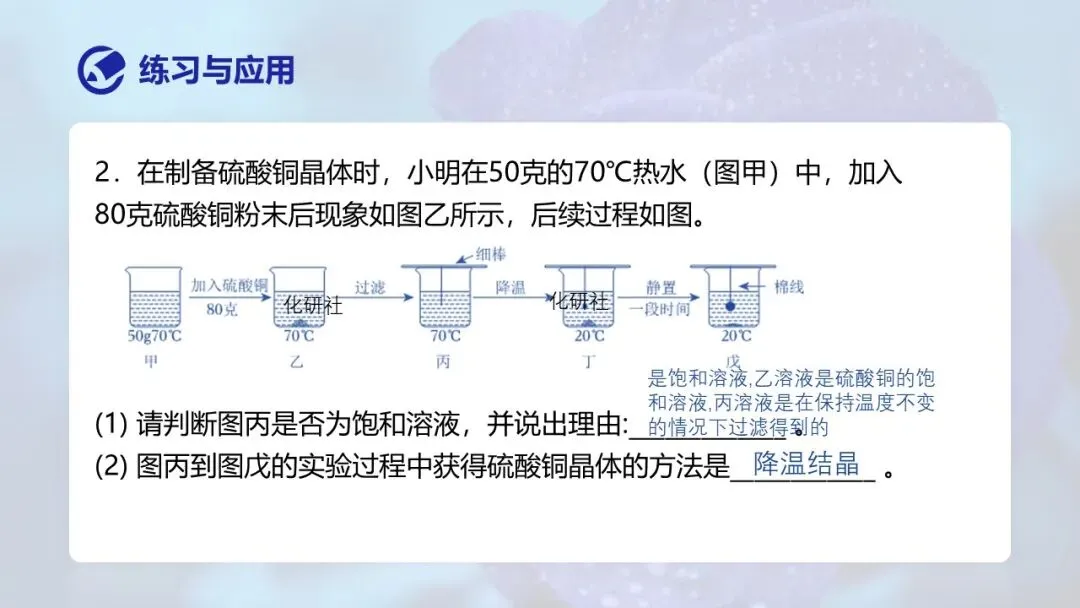
【生5】从硫酸铜溶解度表中还可以发现硫酸铜的溶解度随温度增大而增大,我们可以采用降温结晶获得硫酸铜晶体。
【评价】同学们对于溶解度表不仅会直接查阅溶解度,还从数据变化角度得到结晶方法。
【激疑】如何用50g水配制60℃時硫酸铜饱和溶液呢?
设计意图:利用美丽新奇的“蓝色妖姬——硫酸铜晶体玫瑰花”,激发学生学习的兴趣,让学生在真实情境引导下解决问题。通过探秘“蓝色妖姬——硫酸铜晶体玫瑰花”的制作,复习溶液组成、溶解度相关概念,运用溶解度表解决相关问题,诊断并发展学生的认知水平、提升学生化学学科素养。
环节二创造美——体验溶液的配制
【任务单2】
问题1:配制60℃时硫酸铜饱和溶液具体步骤有哪些?
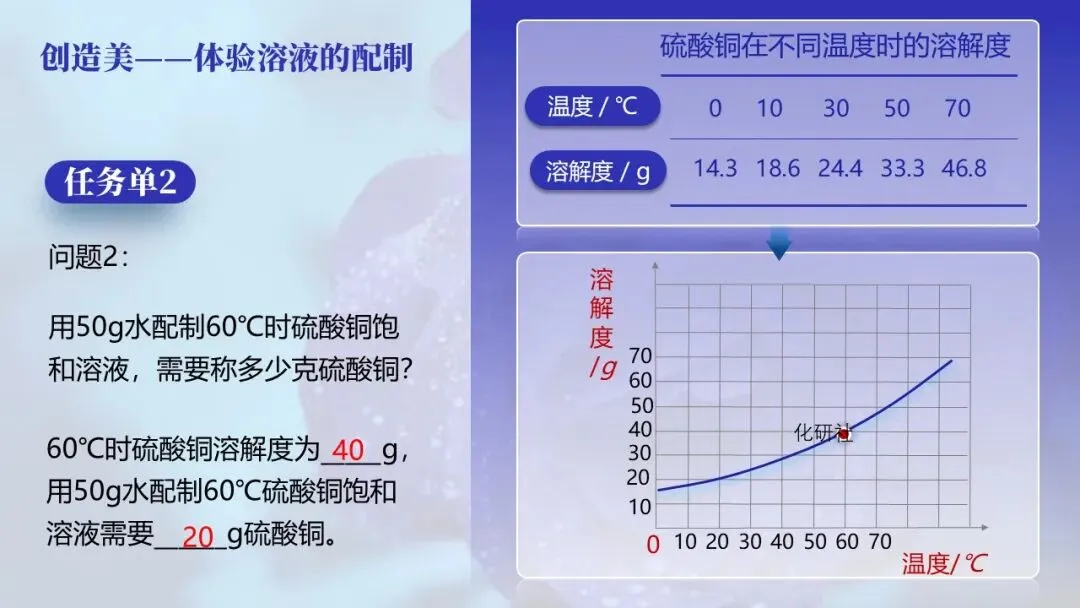
问题2:用50g水配制60℃时硫酸铜饱和溶液,需要称多少克硫酸铜?
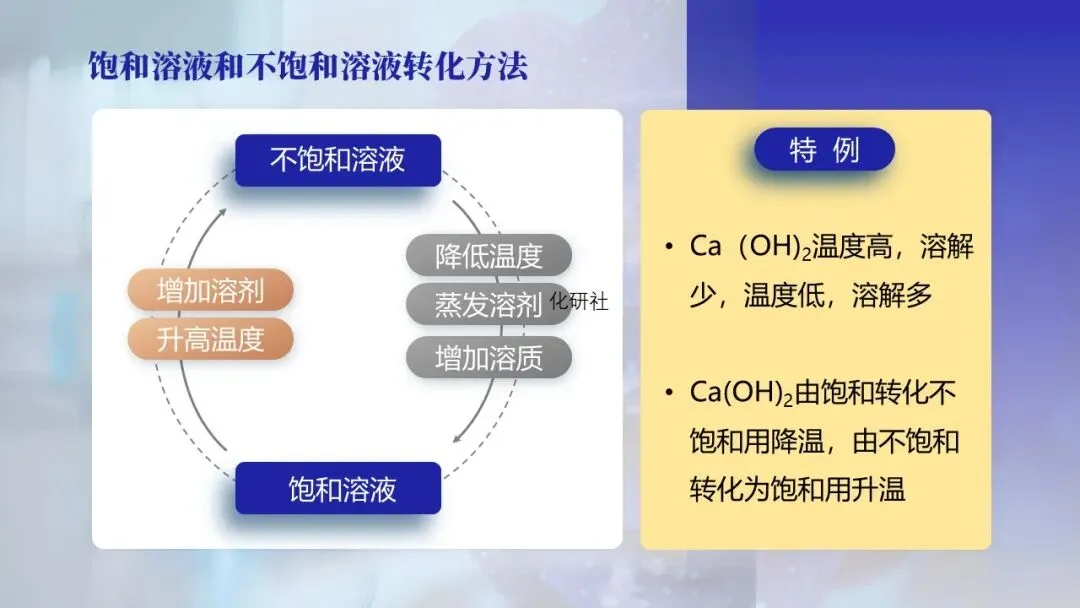
问题3:如何让不饱和溶液变为饱和溶液?
实验探究:用50g水配制60℃时硫酸铜饱和溶液
【生6】配制60℃时硫酸铜饱和溶液具体步骤有计算、称量、溶解和转移。
【生7】用50g水配制60℃时硫酸铜饱和溶液,需要知道60℃时硫酸铜溶解度才能计算硫酸铜的量。
【追问】如何得知60℃时硫酸铜溶解度?
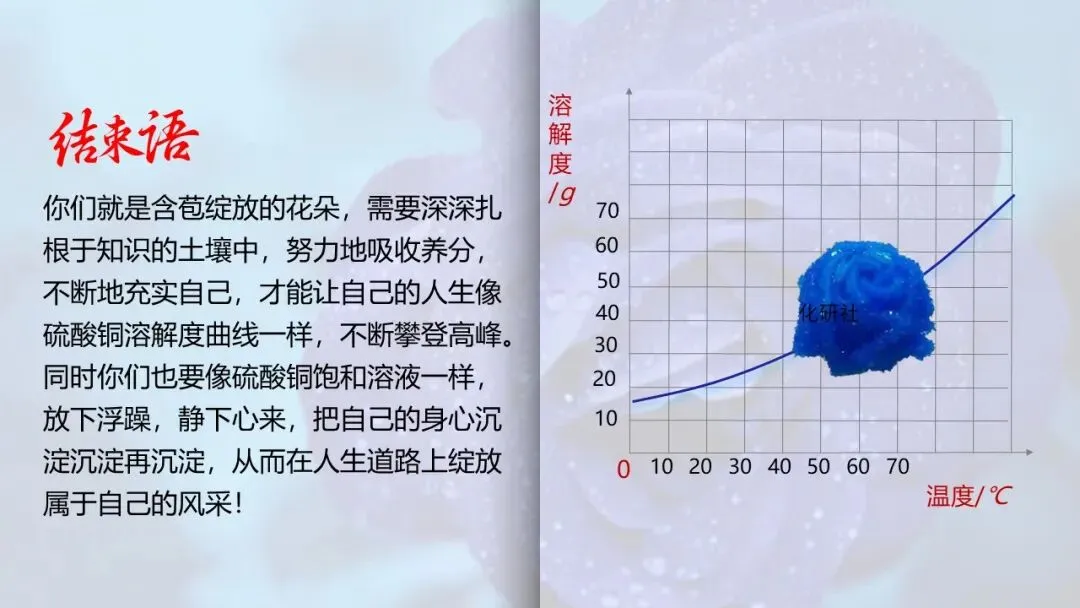
【生8】用硫酸铜溶解度表数据描点作图获得溶解度曲线,可查得60℃时硫酸铜溶解度。
【学生活动1】画硫酸铜溶解度表,查得60℃时硫酸铜溶解度并计算需要硫酸铜的量。
【生9】60℃时硫酸铜溶解度为40g,用50g水配制60℃硫酸铜饱和溶液需要20g硫酸铜。
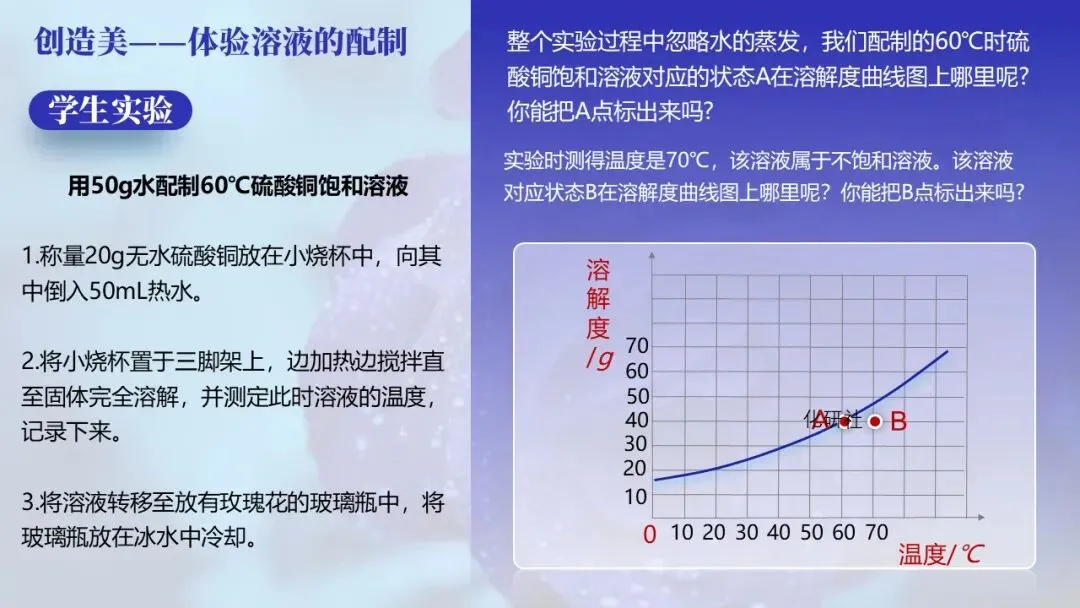
【学生实验】用50g水配制60℃硫酸铜饱和溶液
1.称量20g无水硫酸铜放在小烧杯中,向其中倒入50mL热水。
2.将小烧杯置于三脚架上,边加热边搅拌直至固体完全溶解,并测定此时溶液的温度,记录下来。
3.将溶液转移至放有玫瑰花的玻璃瓶中,将玻璃瓶放在冰水中冷却
......







