中考化学答题技巧3-----坐标曲线题
四季读书网
47
借助于数学方法中的坐标图,把多个因素对体系变化的影响,用坐标图的形式直观地表示出来,学生看图、识图、发掘图形的隐含性质和相互联系的能力是近几年中考的重点方向之一。中考中主要从以下几个方面进行考查,一是与溶解度相关的坐标曲线;二是金属与酸、盐反应坐标曲线;三是pH的变化;四是化学反应中物质质量变化坐标曲线。设问形式主要有:溶液(或溶质、溶剂)质量是多少、浓度是否相等;溶解度是多少、溶解度比较、升降温后溶液成分变化情况分析、提纯或获取晶体的方法、金属的活动性强弱;产生氢气质量大小比较;PH的改变情况;反应后(反应一段时间),溶液的成分等。


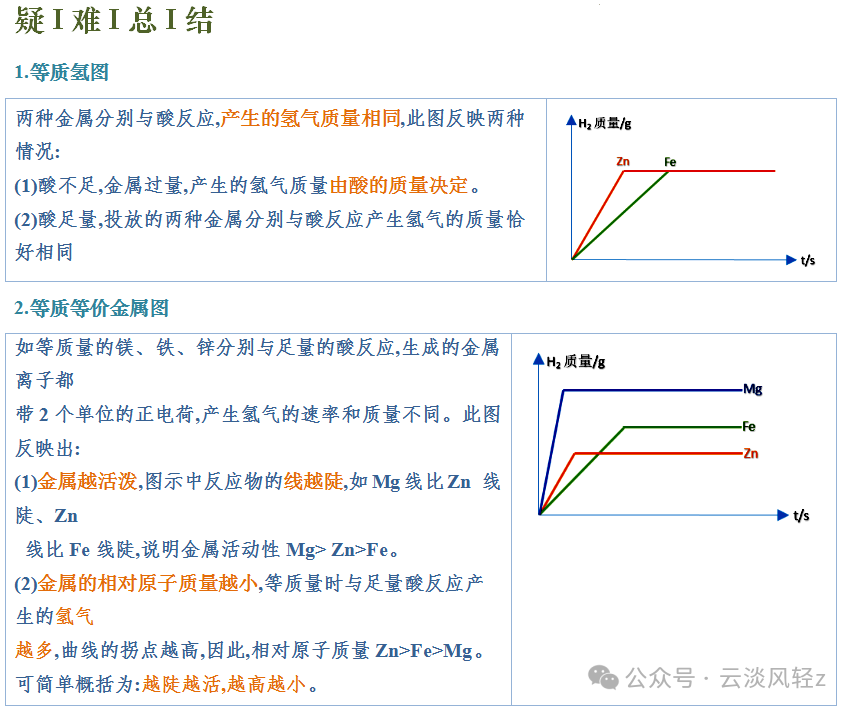

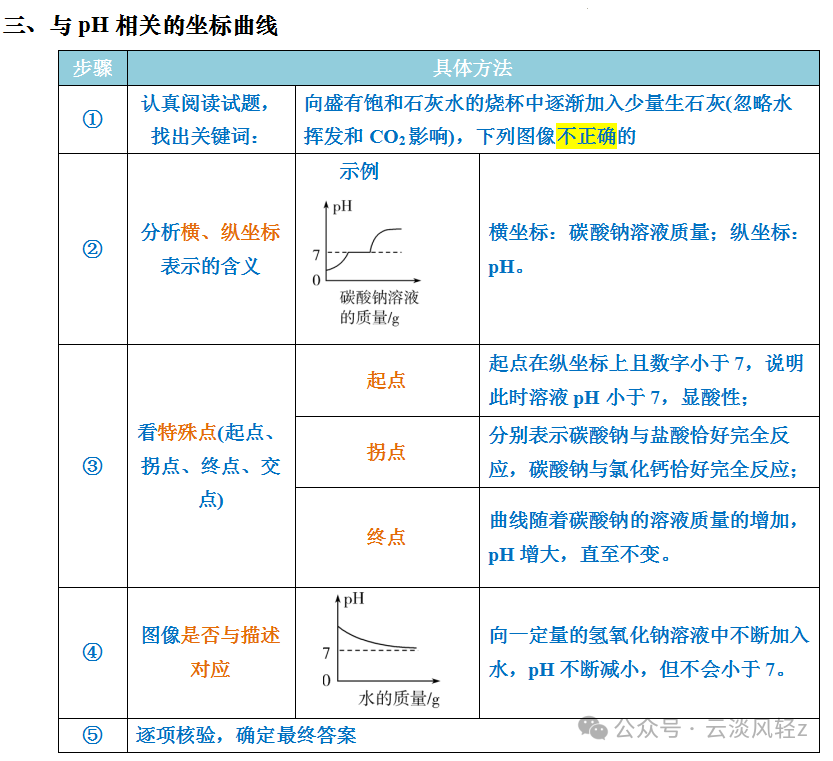
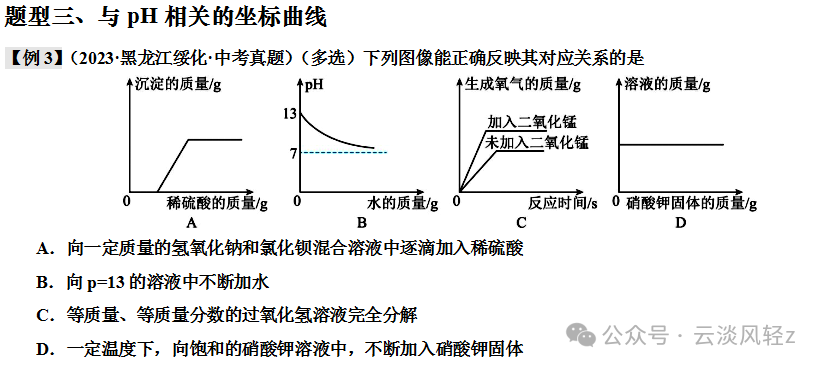
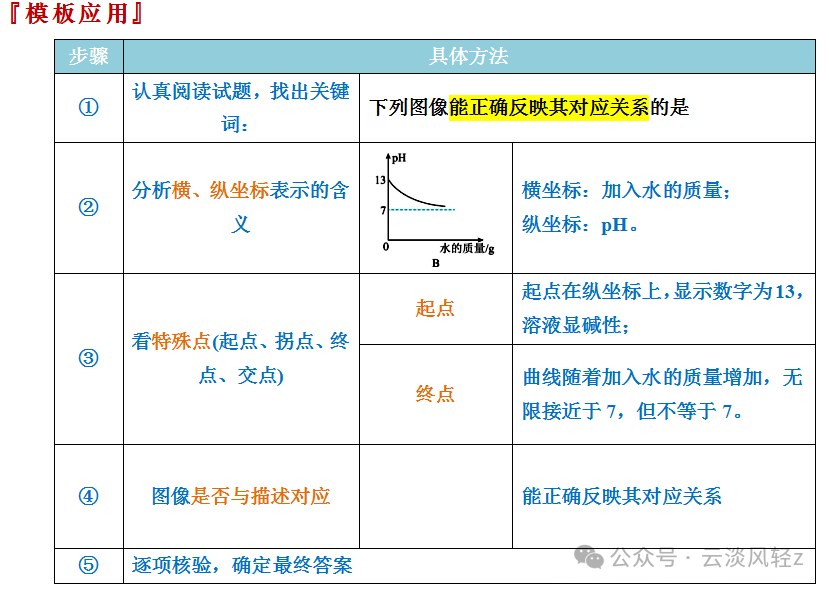
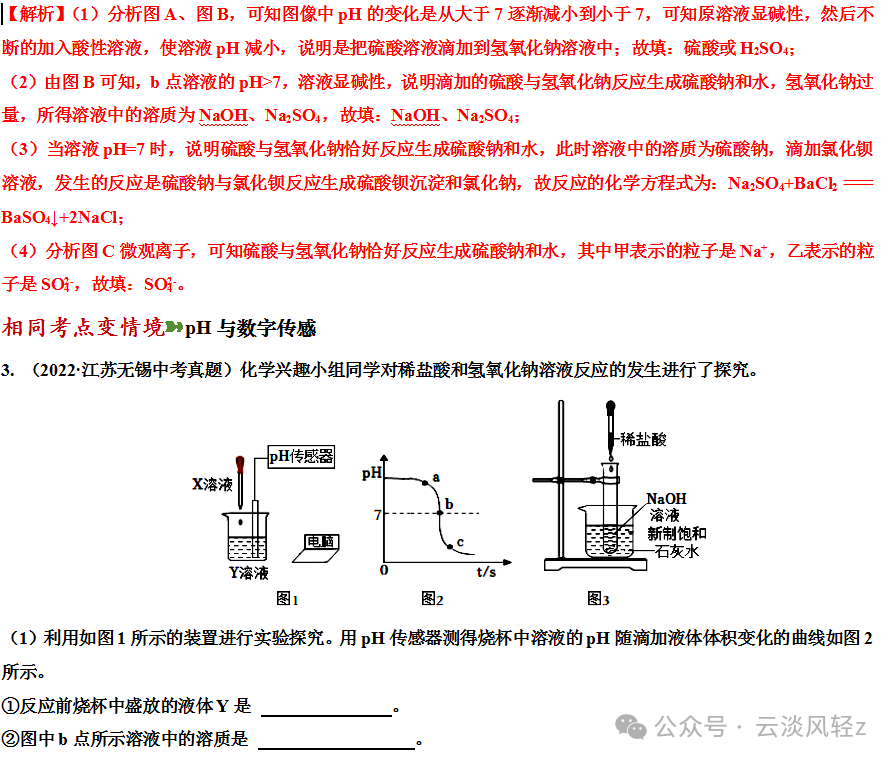
③酸溶液一定显酸性,但显酸性的溶液不一定是酸溶液,如硫酸铵溶液显酸性,但硫酸铵是盐。③碱溶液一定显碱性,但显碱性的溶液不一定是碱溶液,如碳酸钠溶液显碱性,但碳酸钠是盐。因酸性溶液的pH<7,水的pH=7,随着加入水的质量的增加,pH不断增大,但不会大于7因碱性溶液的pH>7,水的pH=7,随着加入水的质量的增加,pH不断减小,但不会小于7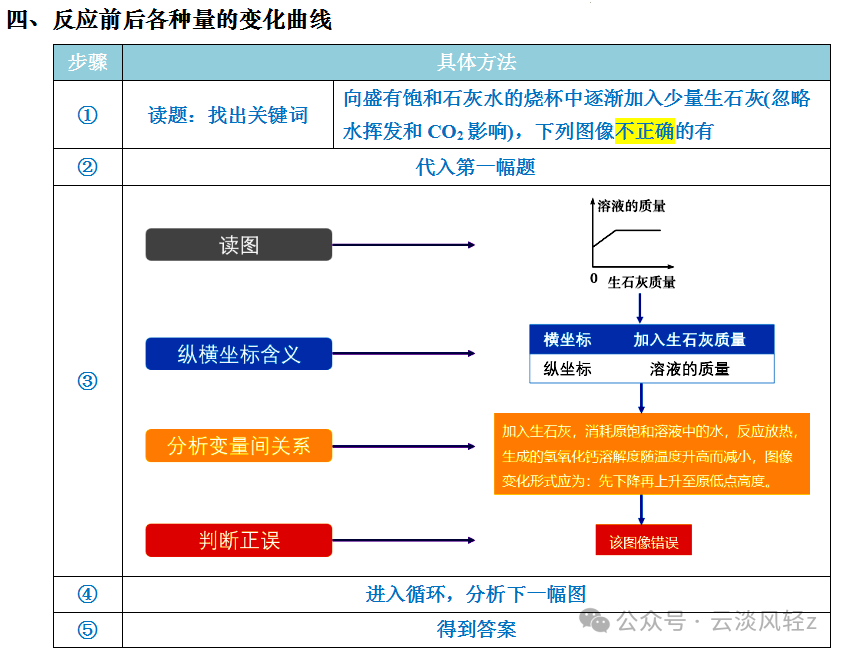
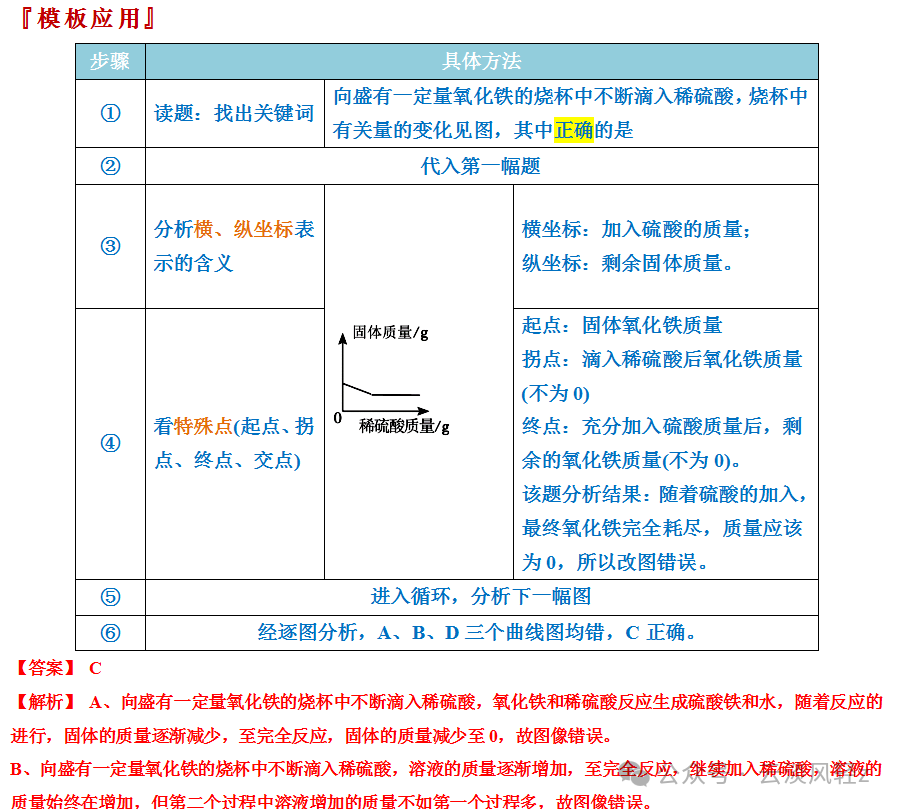
1. 在密闭容器中,随着反应的进行,反应物和生成物的质量总和、元素的种类和质量不会发生变化。2. 催化剂在反应前后质量不变,但在固体混合物中其质量分数一般会发生改变。3. 在非密闭容器中,随着反应的进行,反应物和生成物的质量总和不一定不变。如生成气体或沉淀,原混合物中含有不溶性杂质等变量因素时,要减去这些物质质量。4. 当多种物质可以与某一物质发生反应时,要考虑到反应中存在竞争机制,这会关系到曲线的起点的位置。5. 完全反应后,若继续加入某物质,溶液质量一定变、某溶质质量可能不变,但溶剂质量一般会变。
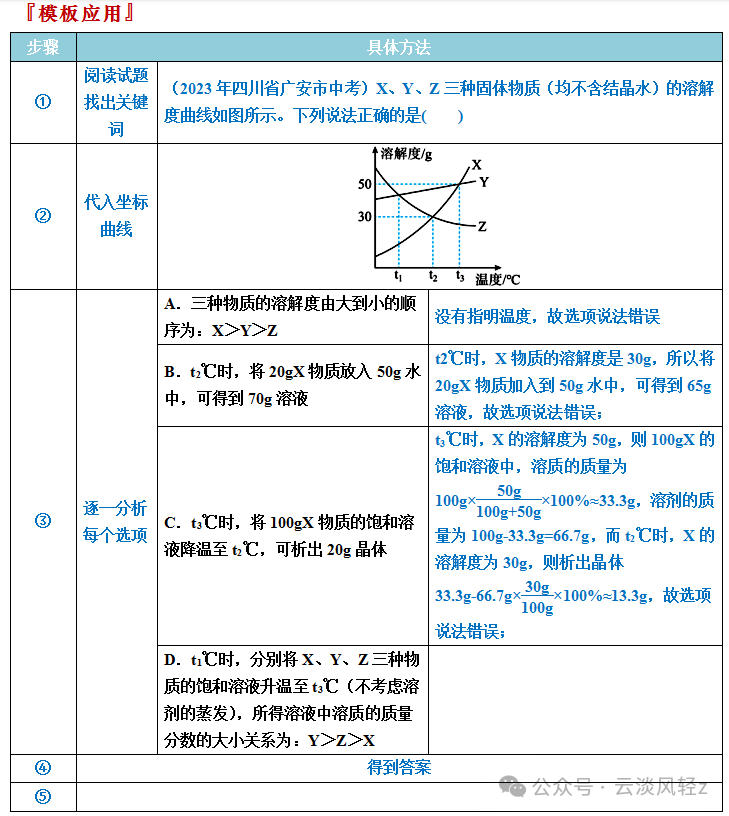
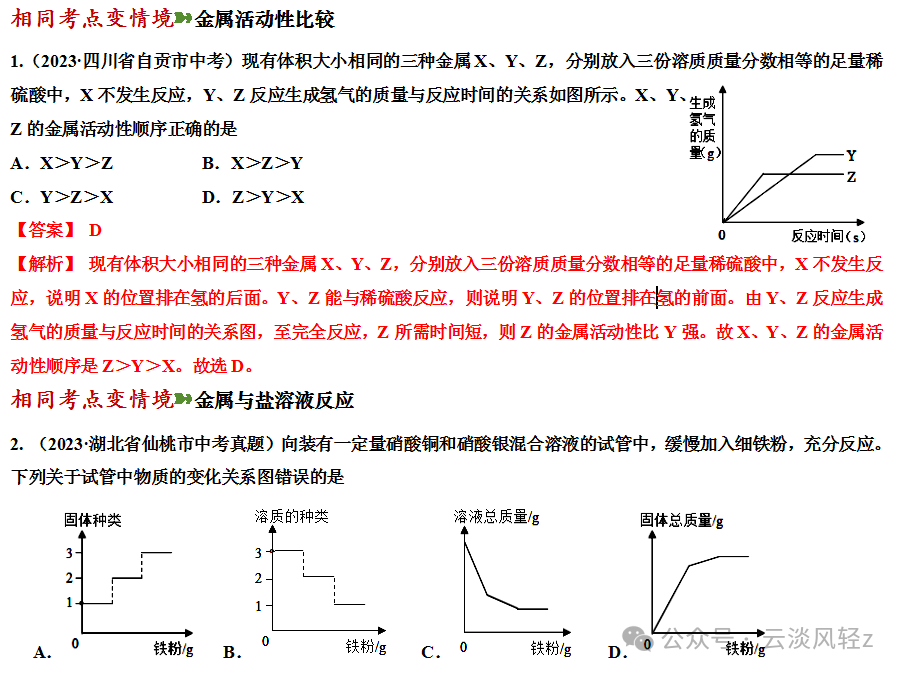
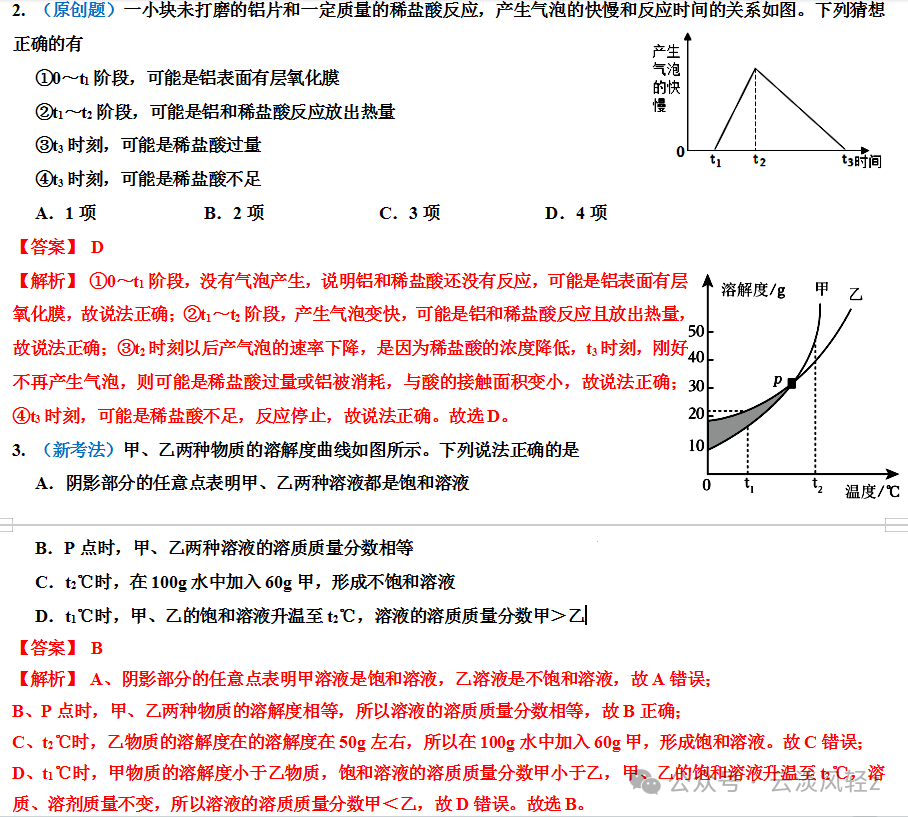
【解析】A、通过分析溶解度曲线可知,t3℃时,三种物质的溶解度的大小关系是X>Y>Z,没有指明温度,故选项说法错误;B、t2℃时,X物质的溶解度是30g,所以将20gX物质加入到50g水中,可得到65g溶液,故选项说法错误;C、t3℃时,X的溶解度为50g,则100gX的饱和溶液中,溶质的质量为100g×100g+50g×100%≈33.3g,溶剂的质量为100g-33.3g=66.7g,而t2℃时,X的溶解度为30g,则析出晶体33.3g-66.7g×100g×100%≈13.3g,故选项说法错误;D、将t1℃时,X、Y、Z三种物质的饱和溶液升温至t3℃,X和Y的溶解度增大,故溶液组成不变,仍然是Y的溶质质量分数大于X,而Z的溶解度减小会析出晶体导致溶质质量分数减小,但大于X,故所得溶液中溶质的质量分数由大到小的顺序是Y>Z>X,故选项说法正确。




























版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容, 请发送邮件至23467321@qq.com举报,一经查实,本站将立刻删除;如已特别标注为本站原创文章的,转载时请以链接形式注明文章出处,谢谢!


















































