
第六部分化学方程式核心知识
一、中考备考指南
1.中考考情分析
(1)核心题型:包含选择、填空简答、物质推断与实验探究题,选择题辨析方程式书写、反应类型及质量守恒定律应用;填空简答要求书写配平方程式、结合微观示意图分析并补全方程式;物质推断以方程式为转化线索推断物质;实验探究结合实验原理书写方程式、验证质量守恒定律。
(2)题型与分值:全国中考普遍占分15~25分,占比极高,全题型覆盖:选择题(2~4道,占比30%,考查质量守恒应用、方程式正误判断、微观示意图、反应类型)、填空题(占比35%,考查方程式规范书写、配平)、实验探究题(占比20%,考查质量守恒定律的验证与变式探究)、计算题(占比15%,核心考查化学方程式的综合计算)。
(3)考查特点:基础知识点以识记、理解为主,核心考查知识的应用能力;难度梯度清晰,基础题占比70%,中档题(实验探究、信息方程式)占比20%,难题(综合计算、守恒法综合应用)占比10%,是中考拉分的核心专题之一。
(4)命题趋势:紧密结合时事热点(航天反应、新能源反应、环保处理反应等)考查陌生信息方程式书写;强化微观示意图与质量守恒定律的结合考查;增加质量守恒定律的实验变式探究;侧重守恒法(元素守恒、原子守恒)在计算中的综合应用;弱化复杂计算,强化计算的规范性与实际场景结合。
2.中考复习要求
(1)一轮复习以夯实基础为核心,深刻理解质量守恒定律的定义、微观本质,熟练掌握其核心应用,无知识盲区;
(2)熟练掌握化学方程式的书写原则、步骤、配平方法,能规范书写初中必考化学方程式,能根据信息书写陌生化学方程式,杜绝书写错误;
(3)精准区分四大基本反应类型,能快速判断反应类型,掌握各类反应的通式与规律;
(4)熟练掌握化学方程式计算的规范步骤与解题方法,能应对基础计算与综合计算,规范答题格式,避免步骤扣分;
(5)掌握质量守恒定律验证实验的操作、现象、误差分析与装置改进,能应对实验变式探究;
(6)熟练运用守恒法(原子守恒、元素守恒、质量守恒)解决各类题型,提升解题速度与准确率。
3.变式出题方向
(1)微观示意图类:结合微观反应示意图,考查质量守恒定律的微观本质、方程式书写、反应类型判断、物质分类;
(2)实验探究类:质量守恒定律的验证实验变式(装置改进、误差分析、异常现象探究);
(3)信息方程式类:结合时事热点、科技前沿,给出反应物、生成物与反应条件,考查陌生化学方程式的书写与配平;
(4)表格数据类:通过反应前后各物质的质量变化表格,考查反应物、生成物的判断、反应类型、质量比计算、未知量求解;
(5)守恒法综合类:结合元素守恒、原子守恒,考查化学式推断、元素质量计算、混合物成分计算;
(6)跨专题综合类:结合金属、酸碱盐、化学与能源等专题,综合考查方程式书写、反应规律与计算。
二、核心知识点梳理
1.质量守恒定律
核心内容:参加反应的各物质质量总和等于生成物质量总和
微观本质:反应前后原子种类、数目、质量均不变
应用范围:解释反应现象、推断物质组成、配平及计算
2.化学方程式书写
书写原则:以客观事实为基础,遵守质量守恒定律
书写步骤:写化学式、配平、标注反应条件及气体沉淀符号
配平方法:最小公倍数法、奇数配偶法、观察法
反应条件:点燃、加热(△)、高温、催化剂等,不能遗漏
特殊符号:气体符号↑、沉淀符号↓,严格遵循使用规则
3.化学方程式的意义
质的意义:明确反应物、生成物、反应条件
量的意义:表示各物质的质量比、粒子个数比
4.化学方程式计算
计算依据:化学反应中各物质质量比固定
规范步骤:设、写、找、列、求、答
注意事项:代入纯净物质量,单位统一
常见题型:基础计算、含杂质计算、表格或图像类计算、综合计算
核心要求:方程式必须配平、相对分子质量计算准确、单位统一、格式规范
✅ 高频考点:质量守恒定律适用于所有化学变化,核心是化学反应前后原子的种类、数目、质量均不变,常用来推断未知物化学式、计算反应物或生成物质量、验证反应前后质量关系;化学方程式需遵循客观事实与质量守恒两大原则,高频考查方程式的书写、配平、含义解读,以及依据方程式进行的相关比例计算。
易错点:易把物理变化归为质量守恒适用范围,混淆反应前后原子不变与分子不变;书写方程式时常出现配平错误、漏标或错标反应条件、气体或沉淀符号使用不当,甚至违背客观事实编造化学式;计算时易算错相对分子质量总和、混淆质量比与体积比,有气体参与或生成的实验未密闭容器,会错误判断质量变化,推算化学式时也常出现原子个数配比错误。
三、中考典型例题
【例题1】(2025·全国中考通用改编)下列化学方程式书写正确的是( )
A.铁在氧气中燃烧:4Fe+3O2点燃2Fe2O3
B.过氧化氢分解:H2O2 MnO2H2↑+O2↑
C.氢氧化钠与盐酸反应:NaOH+HCl=NaCl+H2O
D.铜与稀硫酸反应:Cu+H2SO4=CuSO4+H2↑
【解答】
A选项:铁在氧气中燃烧生成四氧化三铁,不是氧化铁,违背客观事实,正确方程式为3Fe+2O2 点燃Fe3O4,错误;
B选项:过氧化氢分解生成水和氧气,不是氢气和氧气,违背客观事实,正确方程式为2H2O2 MnO22H2O+O2↑,且未配平,错误;
C选项:氢氧化钠与盐酸发生中和反应生成氯化钠和水,化学式正确、配平完整、条件规范,符合书写要求,正确;
D选项选项:铜的金属活动性排在氢之后,不能与稀硫酸发生置换反应,违背客观事实,错误。
答案:C
【分析】
核心知识点:本题考查化学方程式的正误判断,覆盖书写原则、客观事实、配平、反应规律四大核心考点,是中考必考基础题型;
易错点:生成物化学式错误、反应不符合客观规律、未配平、条件遗漏;
踩分点:牢记方程式正误判断四步走:查化学式→查配平→查条件→查符号,同时掌握常见反应的客观规律。
【例题2】(2025·成都中考改编)在密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 20 | 5 | 3 | 32 |
反应后质量/g | 待测 | 25 | 3 | 12 |
A.该反应是分解反应
B.丙一定是该反应的催化剂
C.反应后甲的待测质量为0
D.反应中乙和丁的质量比为5:4
【解答】
根据质量守恒定律,反应前后总质量不变,可得:20+5+3+32=待测+25+3+12,解得待测=20。
反应前后质量变化:乙质量增加20g,是生成物;丁质量减少20g,是反应物;甲、丙质量不变,可能是催化剂,也可能是不参与反应的杂质。
A选项:该反应是丁→乙,符合“一变多”,属于分解反应,正确;
B选项:丙质量不变,可能是催化剂,也可能是不参与反应的杂质,错误;
C选项:待测质量为20,不是0,错误;
D选项选项:乙和丁的质量比为20g:20g=1:1,不是5:4,错误。
答案:A
【分析】
核心知识点:本题考查质量守恒定律的表格类应用,涉及反应物生成物判断、反应类型、催化剂、质量比计算,是中考高频题型;
易错点:总质量计算错误、反应物生成物判断错误、催化剂的界定错误;
踩分点:牢记“质量增加为生成物,质量减少为反应物,质量不变可能为催化剂或杂质”,结合质量守恒定律计算未知量。
【例题3】(2025·重庆中考改编)如图是某化学反应的微观示意图,下列说法错误的是( )
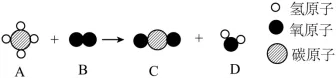
A.该反应前后原子的种类、数目均不变
B.该反应中反应物是甲烷和氧气,生成物是二氧化碳和水
C.该反应属于置换反应
D.该反应中参加反应的甲烷和氧气的质量比为1:4
【解答】
根据微观示意图,该反应是甲烷燃烧,化学方程式为CH4+2O2 点燃CO2+2H2O。
A选项:根据质量守恒定律,化学反应前后原子的种类、数目、质量均不变,正确;
B选项:根据微观示意图,反应物为甲烷和氧气,生成物为二氧化碳和水,正确;
C选项:置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,该反应的生成物是两种化合物,不属于置换反应,错误;
D选项选项:参加反应的甲烷和氧气的质量比为(12+1×4):(2×16×2)=16:64=1:4,正确。
答案:C
【分析】
核心知识点:本题结合微观示意图,考查质量守恒定律的微观本质、化学方程式书写、反应类型判断、质量比计算,是中考必考高频题型;
易错点:反应类型的界定、质量比与分子个数比混淆、微观示意图的信息提取错误;
踩分点:先根据微观示意图写出正确的化学方程式,再结合方程式分析各选项,牢记四大基本反应类型的通式。
【例题4】(2025·北京中考改编)写出下列反应的化学方程式:
(1)红磷在空气中燃烧:______;
(2)实验室用高锰酸钾制取氧气:______;
(3)铁与硫酸铜溶液反应:______;
(4)碳酸钠与稀盐酸反应:______;
(5)二氧化碳通入澄清石灰水:______。
【解答】
(1)红磷在空气中燃烧生成五氧化二磷,化学方程式:4P+5O2点燃2P2O5;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,化学方程式:2KMnO4 加热K2MnO4+MnO2+O2↑;
(3)铁与硫酸铜反应生成硫酸亚铁和铜,化学方程式:Fe+CuSO4=FeSO4+Cu;
(4)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(5)二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O。
【分析】
核心知识点:本题考查初中化学必考核心化学方程式的规范书写,覆盖四大基本反应类型,是中考必考基础题型;
易错点:化学式书写错误、未配平、反应条件遗漏、↑↓符号使用不规范;
扣分点:化学式错误、未配平直接0分,条件、符号错误扣1分,需严格规范书写。
【例题5】(2025·广东中考改编)某同学为验证质量守恒定律,设计了如图所示的实验,请回答下列问题:
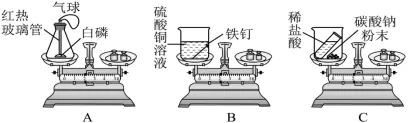
(1)图A是红磷燃烧验证质量守恒定律的实验,实验中气球的作用是______;实验过程中观察到气球的变化是______;反应的化学方程式为______。
(2)图B是铁钉与硫酸铜溶液反应的实验,反应前天平平衡,将铁钉浸入硫酸铜溶液中,充分反应后,观察到的现象是______,天平______(填“平衡”或“不平衡”),该反应______(填“符合”或“不符合”)质量守恒定律。
(3)图C是盐酸与碳酸钠反应的实验,反应前天平平衡,充分反应后,天平指针向______(填“左”或“右”)偏转,原因是______;该反应______(填“符合”或“不符合”)质量守恒定律,若要使天平保持平衡,改进措施是______。
(4)通过上述实验,你得到的启示是:验证质量守恒定律时,对于有气体参与或生成的反应,必须在______容器中进行。
【解答】
(1)气球的作用是平衡装置内外压强,防止胶塞被冲开;红磷燃烧放热,装置内压强增大,气球膨胀,反应结束后温度降低,氧气被消耗,压强减小,气球变瘪,因此气球变化是先膨胀后变瘪;反应的化学方程式为4P+5O2点燃2P2O5。
(2)铁与硫酸铜反应生成硫酸亚铁和铜,观察到的现象是铁钉表面有红色固体析出,溶液由蓝色逐渐变为浅绿色;反应前后没有气体参与或生成,装置内总质量不变,因此天平平衡,该反应符合质量守恒定律。
(3)盐酸与碳酸钠反应生成二氧化碳气体,气体逸散到空气中,左盘质量减小,因此天平指针向右偏转;原因是反应生成的二氧化碳气体逸散到空气中,导致左盘总质量减小;所有化学变化都符合质量守恒定律,因此该反应符合质量守恒定律;改进措施是将反应放在密闭容器中进行。
(4)启示是:验证质量守恒定律时,对于有气体参与或生成的反应,必须在密闭容器中进行。
【分析】
核心知识点:本题考查质量守恒定律的验证实验,覆盖实验操作、现象描述、误差分析、装置改进,是中考实验题高频考点;
易错点:气球变化的描述、天平偏转的原因分析、质量守恒定律的适用范围理解错误;
扣分点:现象描述不完整、原因分析不严谨、化学方程式书写不规范。
【例题6】(2025·全国中考通用改编)实验室用13g锌粒与足量的稀硫酸反应制取氢气,计算:
(1)生成氢气的质量是多少?
(2)理论上可得到硫酸锌的质量是多少?
(已知:Zn+H2SO4=ZnSO4+H2↑)
【解答】
解:(1)设生成氢气的质量为x,生成硫酸锌的质量为y。
Zn+H2SO4=ZnSO4+H2↑
65 161 2
13g y x
65/2=13g/x
x=2×13g/65=0.4g
(2)65/161=13g/y
y=161×13g/65=32.2g
答:(1)生成氢气的质量为0.4g;(2)生成硫酸锌的质量为32.2g。
【分析】
核心知识点:本题考查化学方程式的基础计算,覆盖规范步骤、相对分子质量计算、比例式求解,是中考计算题必考基础题型;
易错点:设未知数带单位、方程式未配平、相对分子质量计算错误、比例式列反、单位不统一;
扣分点:步骤不完整、格式不规范、计算结果错误,需严格遵循“设→写→找→列→解→答”的规范步骤。
四、易错警示与满分话术
1.高频易错点(错例+规范纠正,全板块覆盖)
核心板块 | 典型错例 | 规范纠正 |
质量守恒定律 | 10g水蒸发成10g水蒸气,符合质量守恒定律 | 质量守恒定律只适用于化学变化,物理变化不能用质量守恒定律解释 |
质量守恒定律 | 蜡烛燃烧后质量减少,不符合质量守恒定律 | 所有化学变化都符合质量守恒定律,蜡烛燃烧生成的二氧化碳和水蒸气逸散到空气中,导致剩余固体质量减少,总质量不变 |
质量守恒定律 | 化学反应前后分子的种类、数目、质量均不变 | 化学反应前后,原子的种类、数目、质量均不变;分子种类一定改变,分子数目可能改变 |
质量守恒定律 | 反应前后各物质的质量总和相等,符合质量守恒定律 | 必须是参加化学反应的各物质质量总和,等于反应后生成的各物质质量总和,过量的、未参与反应的物质质量不计入 |
质量守恒定律 | 有气体生成的反应,在敞口容器中进行,天平不平衡,不符合质量守恒定律 | 所有化学变化都符合质量守恒定律,气体逸散导致质量减少,需在密闭容器中验证 |
化学方程式书写 | 铁与稀盐酸反应:2Fe+6HCl=2FeCl3+3H2↑ | 铁与稀酸发生置换反应生成亚铁盐,正确方程式:Fe+2HCl=FeCl2+H2↑,不能臆造生成物 |
化学方程式书写 | 过氧化氢分解:H2O2MnO2H2O+O2 | 方程式未配平,正确方程式:2H2O2MnO22H2O+O2↑,必须遵守质量守恒定律 |
化学方程式书写 | 硫在氧气中燃烧:S+O2点燃SO2↑ | 反应物中有气体,生成物中的气体不能标↑,正确方程式:S+O2点燃SO2 |
化学方程式书写 | 氢氧化钠与硫酸铜反应:2NaOH+CuSO4=Cu(OH)2+Na2SO4 | 生成物氢氧化铜是沉淀,需标↓,正确方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 |
化学方程式书写 | 镁条燃烧:Mg+O2燃烧MgO2 | 两处错误:反应条件是“点燃”不是“燃烧”,氧化镁化学式为MgO,正确方程式:2Mg+O2点燃2MgO |
反应类型判断 | 一氧化碳还原氧化铜:CO+CuO加热Cu+CO2,属于置换反应 | 置换反应是单质+化合物→新单质+新化合物,该反应反应物是两种化合物,不属于置换反应 |
化学方程式计算 | 设生成氢气的质量为x g | 设未知数时不能带单位,正确表述:设生成氢气的质量为x |
化学方程式计算 | 用20g含杂质20%的石灰石与足量稀盐酸反应,直接用20g代入方程式计算 | 必须用纯净物的质量代入方程式计算,纯净物质量=20g×(1-20%)=16g |
2.中考满分表述模板(全板块覆盖,规范答题不扣分)
(1)质量守恒定律规范表述
质量守恒定律定义规范表述:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
质量守恒定律微观本质规范表述:化学反应的过程,就是参加反应的各物质的原子重新组合而生成其他物质的过程。在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
质量守恒定律验证实验现象规范表述:
红磷燃烧实验:红磷燃烧,产生大量白烟,放出热量,气球先膨胀后变瘪,冷却至室温后,天平保持平衡。
铁钉与硫酸铜反应实验:铁钉表面有红色固体析出,溶液由蓝色逐渐变为浅绿色,天平保持平衡。
天平偏转原因规范表述:反应生成的XX气体逸散到空气中,导致左盘总质量减小,天平指针向右偏转;所有化学变化都符合质量守恒定律。
实验改进措施规范表述:将反应放在密闭容器中进行,防止气体逸散,使反应在密闭体系中完成,验证质量守恒定律。
(2)化学方程式书写规范模板
1.写:正确写出反应物、生成物的化学式,中间用短线连接;
2.配:配平化学方程式,使反应前后各原子的种类、数目完全相等,将短线改为等号;
3.注:标注反应条件(点燃、加热△、高温、催化剂等),正确标注↑、↓符号;
4.查:检查化学式是否正确、是否配平、条件是否正确、符号是否规范。
(3)化学方程式计算规范步骤模板
1.设:根据题意设未知量(未知数不带单位);
2.写:正确书写反应的化学方程式(必须配平);
3.找:找出相关物质的相对分子质量总和,对应标出已知量(带单位)、未知量;
4.列:列出比例式(相对分子质量之比等于实际质量之比);
5.解:求解未知量(结果带单位);
6.答:简明写出答案。
(4)反应类型判断规范表述
化合反应:由两种或两种以上物质生成另一种物质的反应,特征是“多变一”。
分解反应:由一种物质生成两种或两种以上其他物质的反应,特征是“一变多”。
置换反应:由一种单质和一种化合物反应,生成另一种单质和另一种化合物的反应,特征是“单换单”。
复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应,特征是“双交换,价不变”。
五、一轮核心必背清单
(一)基础必背(全员过关,全考点覆盖)
质量守恒定律必背
1.核心定义:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
2.微观本质:化学反应前后,原子的种类、数目、质量均不变。
3.核心规律:
五个不变:宏观(元素种类、元素质量、物质总质量不变);微观(原子种类、原子数目、原子质量不变)
两个一定变:宏观(物质种类一定变);微观(分子种类一定变)
一个可能变:分子总数可能变
4.适用范围:只适用于化学变化,不适用于物理变化;只适用于质量守恒,不包括体积守恒。
5.验证实验核心要求:有气体参与或生成的反应,必须在密闭容器中进行。
6.核心应用:解释化学反应中的质量变化、推断化学式、配平方程式、计算质量比、综合计算。
化学方程式必背
1.书写两大原则:以客观事实为基础;遵守质量守恒定律。
2.四大基本反应类型通式:
化合反应:A+B→AB
分解反应:AB→A+B
置换反应:A+BC→B+AC
复分解反应:AB+CD→AD+CB
3.核心配平方法:最小公倍数法、观察法、奇数配偶法。
4.符号使用规则:
↑:反应物中无气体,生成物中有气体,在气体化学式后标注;
↓:在溶液中进行的反应,反应物中无固体,生成物中有固体,在固体化学式后标注;
反应物中的气体、固体,一律不标注↑、↓。
5.方程式正误判断四步走:查化学式→查配平→查条件→查符号。
6.计算核心依据:化学反应中,各物质的质量比等于相对分子质量乘以化学计量数之比,为定值。
初中必考核心化学方程式(分类必背)
1.化合反应
红磷燃烧:4P+5O2点燃2P2O5
硫燃烧:S+O2点燃SO2
碳充分燃烧:C+O2点燃CO2
铁在氧气中燃烧:3Fe+2O2点燃Fe3O4
镁条燃烧:2Mg+O2点燃2MgO
二氧化碳与水反应:CO2+H2O=H2CO3
氧化钙与水反应:CaO+H2O=Ca(OH)2
2.分解反应
过氧化氢分解:2H2O2MnO22H2O+O2↑
高锰酸钾制氧气:2KMnO4加热K2MnO4+MnO2+O2↑
氯酸钾制氧气:2KClO3═══△2KCl+3O2↑
电解水:2H2O通电2H2↑+O2↑
碳酸分解:H2CO3=H2O+CO2↑
碳酸钙高温分解:CaCO3高温CaO+CO2↑
3.置换反应
锌与稀硫酸:Zn+H2SO4=ZnSO4+H2↑
铁与稀盐酸:Fe+2HCl=FeCl2+H2↑
铁与硫酸铜:Fe+CuSO4=FeSO4+Cu
铜与硝酸银:Cu+2AgNO3=Cu(NO3)2+2Ag
氢气还原氧化铜:H2+CuO加热Cu+H2O
碳还原氧化铜:C+2CuO高温2Cu+CO2↑
4.复分解反应
氢氧化钠与盐酸:NaOH+HCl=NaCl+H2O
氢氧化钙与盐酸:Ca(OH)2+2HCl=CaCl2+2H2O
碳酸钠与稀盐酸:Na2CO3+2HCl=2NaCl+H2O+CO2↑
碳酸钙与稀盐酸:CaCO3+2HCl=CaCl2+H2O+CO2↑
氢氧化钠与硫酸铜:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
氯化钠与硝酸银:NaCl+AgNO3=AgCl↓+NaNO3
硫酸钠与氯化钡:Na2SO4+BaCl2=BaSO4↓+2NaCl
5.其他反应
二氧化碳与澄清石灰水:CO2+Ca(OH)2=CaCO3↓+H2O
二氧化碳与氢氧化钠:CO2+2NaOH=Na2CO3+H2O
一氧化碳还原氧化铜:CO+CuO加热Cu+CO2
一氧化碳还原氧化铁:3CO+Fe2O3 高温2Fe+3CO2
甲烷燃烧:CH4+2O2 点燃CO2+2H2O
乙醇燃烧:C2H5OH+3O2 点燃2CO2+3H2O
(二)易错必背(失分重灾区,全板块覆盖)
1.质量守恒定律易错必背
质量守恒定律只适用于化学变化,物理变化不能用其解释;
必须是参加反应的物质质量,过量的、未反应的物质质量不能计入;
有气体参与或生成的反应,计算总质量时必须包含气体的质量,不能忽略;
化学反应前后,原子一定不变,分子一定改变,分子数目可能改变,不能混淆;
元素守恒:化学反应前后,元素的种类、质量一定不变,可用于推断化学式、计算元素质量。
2.化学方程式书写易错必背
化学式必须正确,不能臆造,比如铁与稀酸反应生成亚铁盐(Fe2+),不是铁盐(Fe3+);
反应条件必须准确:“点燃”≠“燃烧”,“加热(△)”≠“高温”,催化剂不能写在反应物或生成物中;
配平必须完整,不能只配平部分原子,配平后各原子的种类、数目必须完全相等;
↑↓符号不能乱用:反应物中有气体或固体,生成物中的气体或固体一律不标;
不能遗漏反应条件和符号,否则中考会扣分。
3.反应类型易错必背
置换反应必须是“单质+化合物→新单质+新化合物”,反应物或生成物没有单质的,一定不是置换反应;
复分解反应必须是“双交换,价不变”,反应前后各元素的化合价一定不变,化合价改变的一定不是复分解反应;
中和反应属于复分解反应,不是基本反应类型;
一氧化碳还原金属氧化物的反应,不属于四大基本反应类型。
4.化学方程式计算易错必背
设未知数时不能带单位,计算结果要带单位;
必须用纯净物的质量代入方程式计算,混合物质量要先换算成纯净物质量(纯净物质量=混合物质量×纯度);
化学方程式必须配平,否则计算结果完全错误;
相对分子质量计算必须准确,要乘以化学计量数;
单位必须统一,体积要先换算成质量(质量=密度×体积);
步骤必须完整,严格遵循“设→写→找→列→解→答”,缺少步骤会扣分。
(三)技巧必背(提速提分,一轮复习速记)
1.化学方程式配平口诀
最小公倍数法:找出两边各出现一次、原子个数差大的元素,求最小公倍数,配平对应原子,再配平其他原子。
奇数配偶法:找两边出现次数最多、原子个数一奇一偶的元素,把奇数变成偶数,再配平其他原子。
观察法:找化学式最复杂的物质,定其计量数为1,再配平其他物质,最后化为整数。
2.方程式正误判断速记口诀
化学式要正确,配平要完整,
条件标准确,符号不乱用。
3.质量守恒表格题解题口诀
增为生成物,减为反应物,
不变可能催化剂,总质量守恒算未知数。
4.微观示意图解题口诀
先写化学式,再配平方程式,
原子全不变,分子可再分,
类型看通式,质量比算清。
5.守恒法解题技巧
原子守恒:化学反应前后原子的种类、数目不变,用于推断化学式、配平方程式;
元素守恒:化学反应前后元素的种类、质量不变,用于计算混合物中元素质量、推断物质组成;
质量守恒:反应前后总质量不变,用于计算未知量、表格题、图像题。
6.化学方程式计算速记口诀
化学式要写对,配平是首位,
相对质量算准确,纯量代方程,
单位要统一,步骤要完整。
六、分层巩固专项训练
1.基础题(8道,复习达标,全考点覆盖)
1.(考点:质量守恒定律的理解)下列现象不能用质量守恒定律解释的是( )
A.红磷燃烧后固体质量增加
B.冰融化成水,质量不变
C.蜡烛燃烧后质量减少
D.高锰酸钾受热分解后固体质量减少
2.(考点:质量守恒定律的微观本质)化学反应前后,一定不变的是( )
①原子种类②分子种类③元素种类④物质种类⑤原子数目⑥分子数目
A.①③⑤
B.①②⑥
C.②③⑤
D.②④⑥
3.(考点:化学方程式正误判断)下列化学方程式书写正确的是( )
A.镁条燃烧:Mg+O2 点燃MgO
B.过氧化氢分解:2H2O2 MnO22H2O+O2↑
C.铁与稀硫酸反应:2Fe+3H2SO4=Fe2(SO4)3+3H2↑
D.碳酸钙与稀盐酸反应:CaCO3+HCl=CaCl2+H2O+CO2↑
4.(考点:基本反应类型判断)下列反应属于置换反应的是( )
A.3CO+Fe2O3 高温2Fe+3CO2
B.2H2O 通电2H2↑+O2↑
C.CO2+2NaOH=Na2CO3+H2O
D.Cu+2AgNO3=Cu(NO3)2+2Ag
5.(考点:质量守恒定律应用·推断化学式)某反应的化学方程式为2X+3O2点燃2CO2+4H2O,则X的化学式为( )
A.CH4
B.C2H5OH
C.CH3OH
D.C2H4
6.(考点:化学方程式的意义)关于2H2+O2 点燃2H2O的说法错误的是( )
A.氢气和氧气在点燃条件下反应生成水
B.反应前后氢元素和氧元素的种类不变
C.反应中氢气、氧气、水的质量比为2:1:2
D.反应中氢分子、氧分子、水分子的个数比为2:1:2
7.(考点:复分解反应的判断)下列物质之间不能发生复分解反应的是( )
A.氢氧化钠溶液和稀盐酸
B.氯化钠溶液和硝酸钾溶液
C.硫酸铜溶液和氢氧化钠溶液
D.碳酸钠溶液和稀硫酸
8.(考点:化学方程式基础计算)实验室用足量的一氧化碳还原8g氧化铜,理论上可得到铜的质量是( )
A.3.2g
B.6.4g
C.8g
D.16g
2.提高题(5道,易错突破,全易错点覆盖)
1.(考点:质量守恒定律表格题)在密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是( )
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 8 | 32 | 5 | 4 |
反应后质量/g | 16 | 4 | x | 24 |
A.x=5,丙一定是该反应的催化剂
B.该反应是化合反应
C.反应中甲和丁的质量比为2:3
D.该反应中乙是生成物
2.(考点:微观示意图)如图是某化学反应的微观示意图,下列说法正确的是( )

A.该反应的反应物是氨气和氧气,生成物是氮气和水
B.该反应属于置换反应
C.反应前后分子的数目不变
D.反应中氨气和氧气的质量比为17:32
3.(考点:质量守恒定律实验探究)下列验证质量守恒定律的实验中,能达到实验目的的是( )
A.红磷燃烧在敞口锥形瓶中进行
B.盐酸与碳酸钠反应在敞口烧杯中进行
C.铁钉与硫酸铜反应在敞口烧杯中进行
D.镁条燃烧在空气中进行
4.(考点:信息方程式书写)2025年我国科学家研发了新型催化剂,可将二氧化碳和氢气在一定条件下转化为甲醇(CH3OH)和水,下列说法正确的是( )
A.该反应的化学方程式为CO2+3H2 催化剂CH3OH+H2O
B.该反应属于分解反应
C.反应前后分子的种类、数目均不变
D.该反应无法缓解温室效应
5.(考点:守恒法综合应用)某有机物在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,下列关于该有机物组成的说法正确的是( )
A.只含有碳、氢两种元素
B.一定含有碳、氢元素,可能含有氧元素
C.一定含有碳、氢、氧三种元素
D.碳、氢元素的质量比为4:1
3.拓展题(1道,能力拔高,综合实验+计算)
(考点:质量守恒定律实验探究+化学方程式综合计算)某化学兴趣小组为验证质量守恒定律,进行了如下实验,并对反应后溶液的溶质成分进行了探究与计算。
【实验1】验证质量守恒定律
(1)小组同学设计了如图所示实验,将盛有稀盐酸的小试管放入盛有大理石的锥形瓶中,称量装置总质量为125.6g,然后将稀盐酸倒入锥形瓶中,充分反应。
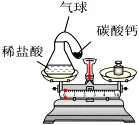
①写出该反应的化学方程式______;
②实验中观察到的现象是______;
③反应结束后,冷却至室温,再次称量装置总质量为125.6g,天平保持平衡,该实验______(填“能”或“不能”)验证质量守恒定律,原因是______。
(2)若将该实验放在敞口烧杯中进行,反应结束后,称量总质量为123.4g,减少的质量是______的质量,该反应______(填“符合”或“不符合”)质量守恒定律。
【实验2】计算反应后溶液的溶质质量分数
(3)将上述125.6g反应后的混合物过滤,得到滤液100g,计算该滤液中氯化钙的质量分数。(已知:大理石中杂质不参与反应,也不溶于水;)
【解答提示】
①结合碳酸钙与稀盐酸的反应,规范书写化学方程式,描述实验现象;
②结合质量守恒定律,分析天平平衡的原因与质量减少的原因;
③先根据质量差计算生成二氧化碳的质量,再结合化学方程式计算氯化钙的质量,最后计算溶质质量分数。
【参考答案】
基础题:1.B 2.A 3.B 4.D 5.C 6.C 7.B 8.B
提高题:1.C 2.A 3.C 4.A 5.B
拓展题
(1)①CaCO3+2HCl=CaCl2+H2O+CO2↑;
②大理石表面有气泡产生,气球膨胀;
③能;反应在密闭容器中进行,反应前后总质量不变,符合质量守恒定律
(2)生成的二氧化碳;符合
(3)解:生成二氧化碳的质量=125.6g-123.4g=2.2g
设生成氯化钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
111 44
x 2.2g
111/44=x/2.2g
x=5.55g
滤液中氯化钙的质量分数=5.55g/100g×100%=5.55%
答:该滤液中氯化钙的质量分数为5.55%。







