(点击查看详情)
中考生物知识点汇总
【中考复习】生物专题知识点①:构成生物体的细胞、组织、器官和系统
【中考复习】生物专题知识点③:种群、群落、和生态系统及生物圈
中考化学考点汇总
备考指南
考点要求 | 课标要求 | 考查频次 | 命题预测 |
金属及其性质 | 1.了解金属的主要物理性质及用途,辨析金属和非 金属。 2.认识常见金属的主要化学性质,知道金属活动性顺序。 3.列举金属锈蚀的条件和防止金属锈蚀的常用方法。 4.知道在一种金属中加入其他金属或非金属形成合金,可以改善金属材料的性能;了解新型金属材料的发展与应用。 5.举例说明金属冶炼技术的发展对社会进步的作用6.了解废弃金属对环境的影响,以及金属回收再利用的意义。 | 24年考查6分 | 1.金属材料的命题点有:①常见金属的物理性质及其应用;②合金及合金的优点;③常见几种合金如钢、生铁、铝合金、不锈钢等的成分和特点等,考察中多在简单的选择题中出现,结合国防、农业、环保等元素. 2.金属的化学性质命题点有:①常见金属和氧气反应及其现象;②常见金属和酸反应及其现象;③通过金属和氧气、酸反应得出比较金属活性的方法等,考察形式多样、在选择、填空、探究、解答题中均可以出现,其中在解答计算题中常用合金为背景,计算其中某金属的质量分数. 3.金属活动顺序与置换反应命题点有:①金属活动顺序关系;②金属活动顺序的意义;③实验探究金属之间的活泼性; 4.金属的腐蚀与防护命题点有:①金属腐蚀的条件;②利用控制变量法探究金属腐蚀的条件;③金属防腐的常用方法等,多在实验探究题中均可以出现 |
知识导图
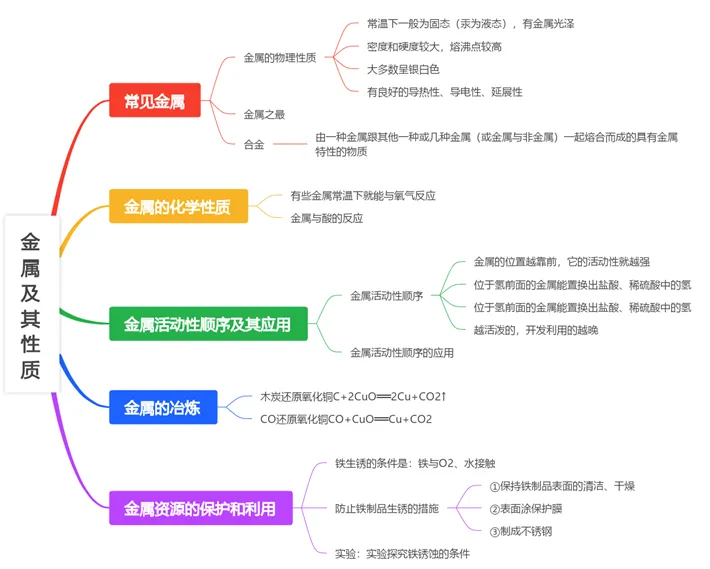
考点梳理
考点一 常见金属

金属材料:一般分为纯金属和合金两类。
1.金属的物理性质:
(1)常温下一般为固态(汞为液态),有金属光泽;
(2)密度和硬度较大,熔沸点较高;
(3)大多数呈银白色(铜为紫红色,金为黄色)
(4)有良好的导热性、导电性、延展性
2.金属之最:
(1)铝:地壳中含量最多的金属元素;
(2)钙:人体中含量最多的金属元素;
(3)铁:目前世界年产量最多的金属(铁>铝>铜);
(4)银:导电、导热性最好的金属(银>铜>金>铝);
考点二 合金

1.定义:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
注意事项:(①合金是金属与金属或金属与非金属的混合物;②金属在熔合了其它金属和非金属后,不仅组成上发生了变化,其内部组成结构也发生了改变,从而引起性质的变化)。
2.合金特点:一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好
3.举例:
(1)铁的合金:生铁(含碳量2%~4.3%)和钢(含碳量0.03%~2%)。区别:含碳量不同
(2)铜合金:黄铜:铜、锌的合金;青铜:铜、锡的合金,它人类使用最早的合金。
(3)钛合金:被认为是21世纪的重要金属材料。
优点:I、熔点高、密度小;
II、可塑性好、易于加工、机械性能好;
III、抗腐蚀性能好;用途:广泛用于喷气式发动机、飞机机身、人造卫星外壳、火箭壳体、医学补形、人造骨、海水淡化设备、海轮、舰艇的外壳等。
(4)铝合金:铝中加入镁、铜、锌等形成合金。广泛应用于制造飞机、舰艇和载重汽车等。
考点三 金属的化学性质

1.有些金属常温下就能与氧气反应
(1)在常温下,金属铝的表面易生成一层致密的氧化铝保护膜,它能阻止金属铝继续被空气氧化,因此铝具有很好的抗腐蚀性能。反应的化学方程式为4A1+3O2 = 2Al2O3
(2)在常温下,铁在潮湿的空气中会被氧化而生锈(铁锈的主要成分是Fe2O3)。
2.有些金属能在空气中燃烧
2Mg+O2点燃2MgO,现象是剧烈燃烧,发出耀眼的白光,生成白色固体(氧化镁),放出热量。3.有些金属在空气中不燃烧,但能在氧气(纯氧)中燃烧
3Fe+2O2点燃Fe3O4,现象是剧烈燃烧,火星四射,生成黑色固体(四氧化三铁),放出热量。
4.有些金属虽不能燃烧,但在加热的条件下能与氧气反应生成氧化物
2Cu+O2△ 2CuO,现象是铜丝表面由紫红色变成黑色。
5.金等金属即使在高温下也不与氧气反应
6.金属与酸的反应
(1)镁、锌等金属能与稀盐酸或稀硫酸发生反应,生成相应的盐和氢气。金属表面会有气泡出现,反应的化学方程式为
Mg+2HCl = MgCl2+H2↑
Zn+2HCl = ZnCl2+H2↑
Mg+H2SO4= MgSO4+H2↑
Zn+H2SO4 = ZnSO4+H2↑
将燃着的木条接近有气泡产生的试管,松开拇指发现气体燃烧,此气体即为氢气。
(2)铜、银等金属不与稀盐酸或稀硫酸反应,放入两种酸中无明显现象。
考点四 金属活动性顺序及其应用

1.金属活动性顺序

在金属活动性顺序里:
(1)金属的位置越靠前,它的活动性就越强
(2)位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)
(3)位于氢前面的金属能置换出盐酸、稀硫酸中的氢。(除K、Ca、Na)
(4)越活泼的,开发利用的越晚。
2.金属活动性顺序的应用
(1)根据所发生反应的情况判断金属的活动性强弱。比较金属活动性的强弱可根据其与氧气反应的难易,与酸反应的快慢、与另一种金属的盐溶液能否发生反应等情况做出判断。
(2)根据金属活动性顺序判断置换反应能否发生。
(3)根据金属活动性顺序判断金属与其他物质发生反应后所得物质的成分。
(4)用于物质除杂试剂的选择。
考点五 金属的冶炼

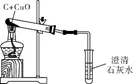
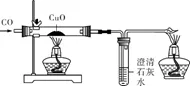
实验 | 木炭还原氧化铜 | CO还原氧化铜 |
实验原理 | C+2CuO══2Cu+CO2↑ | CO+CuO══Cu+CO2 |
实验装置 |
|
|
黑色粉末逐渐变红色,澄清石灰水变浑浊 | ||
注意事项 | (1)试管口应略向下倾斜,目的是防止冷凝水回流到灼热的试管底部,使试管炸裂。 (2)加热时,在酒精灯火焰上加网罩的目的是使火焰集中并提高温度。 (3)加热时,在酒精灯火焰上加网罩的原因是增大药品的加热接触面积,受热均匀,使反应更充分。 (4)反应结束时,先把导管从石灰水中撤出,再停止加热,原因是防止试管中液体倒流,炸裂试管。 | (1)加热前先通一会儿CO,目的是排出装置内的空气,防止CO不纯,加热后发生爆炸。 (2)反应结束后先停止加热,继续通CO至玻璃管冷却的作用是防止灼热的铜重新被氧化。 (3)CO有毒,尾气必须进行处理,通常采用点燃法,防止污染空气 |
考点六 金属资源的保护和利用

1.铁的锈蚀
(1)铁生锈的条件是:铁与O2、水接触(铁锈的主要成分:Fe2O3·xH2O)
(2)防止铁制品生锈的措施:①保持铁制品表面的清洁、干燥;②表面涂保护膜(涂油、刷漆、电镀、烤蓝等);③制成不锈钢;
(3)铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气反应,因此铁制品可以全部被锈蚀。因而铁锈应及时除去。
(4)而铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
实验01实验探究铁锈蚀的条件
(1)实验在3支试管中进行:A试管中是水和空气,B试管中是刚煮沸过的蒸馏水,C试管中是装有干燥剂(生石灰)的干燥空气,在3支试管中各放一枚铁钉,并用塞子塞紧试管口,实验装置图如图所示。
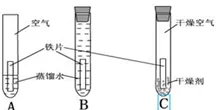
(2)一段时间后A中铁钉锈蚀严重,B、C中铁钉基本不锈蚀,说明铁生锈条件是与水和空气(氧气)同时接触。
(3)因为纯铁和铁钉的内部结构不同,纯铁并未生锈。
2.保护金属资源途径